Lebensstil der Eltern: epigenetische Wirkung auf die Kinder
Wie die Ernährung und der Lebensstil der Eltern ihre ungeborenen Kinder epigenetisch beeinflusst. Wir unterschätzen die epigenetische Wirkung.
Inhaltsverzeichnis
- Fazit
- 1. Die Ernährung der Eltern beeinflusst Gesundheit und Wohlbefinden ihrer Kinder
- 2. Wieso geschieht das?
- 3. Metabolische Ernährungsprogrammierung
- 4. Was passiert auf der zellulären Ebene?
- 5. Epigenetik ist der Hauptprozess der "Ernährungsprogrammierung"
- 6. Wie Ihr Lebensstil die Gesundheit Ihrer Kinder beeinflussen kann
- Literaturverzeichnis
Fazit
Nutritional Programming, also die "Ernährungs-Programmierung", erklärt die Anfälligkeit (Prädisposition) von gewissen Menschen, im Erwachsenenalter verschiedenste Krankheiten zu erleiden. Grund dafür ist vor allem eine veränderte Entwicklung während der fetalen Phase und in der frühen Kindheit.
Laut dem Paradigma von Barker (Entwicklungsbedingter Ursprung von Gesundheit und Erkrankung, im Original: Developmental Origins of Health and Disease) beeinflussen die Bedingungen während der Präkonzeption (2-3 Monate vor der Schwangerschaft) sowie die Schwangerschaft und die Laktationsphase die jeweiligen Individuen sehr stark. Ungünstige Umweltbedingungen verursachen eine Prädisposition für bestimmte, vor allem entzündliche, Krankheiten, die sich später im Erwachsenenleben manifestieren.1
Über- und Unterernährung sind wichtige Einflüsse, die zu einem schädlichen Umfeld für das ungeborene Kind beitragen. Diese hängen direkt mit metabolischen Bedingungen wie Bluthochdruck, Insulinresistenz, Hyperlipämie und abdominaler Fettleibigkeit zusammen.2
Ist die Umwelt schädlich, passt sich der Embryo, der Fötus oder das Neugeborene an, um diese nachteiligen Bedingungen zu überleben. Diese Veränderungen betreffen die Körperfunktionen, den Gewebeumbau und die Aktivierung oder Stummschaltung bestimmter Gene. Sie können dauerhaft bestehen und sogar aktiv bleiben, obwohl die schädlichen Reize verschwunden sind.
Unterernährung während der Schwangerschaft und der frühen Kindheit kann das Risiko für Fettleibigkeit, Diabetes, metabolisches Syndrom und Herz-Kreislauf-Erkrankungen im späteren Leben erhöhen. Vorausgesetzt, Sie ernähren sich ungesund und weisen eine niedrige körperliche Aktivität auf.3
Ein kurzes Glossar
Embryo: Wenn das Ei vom Spermium befruchtet ist (Zygote), beginnt es sich zu teilen, um einen Zellball (Blastozyste) zu formen und sich dann in den Uterus zu bewegen. Hier bildet ein Teil dieser Zellen die Plazenta, während sich die anderen zum Embryo entwickeln. In diesem Stadium bilden sich die meisten inneren Organe und die Körperstruktur. Die Entwicklung des Gehirns und des Rückenmarks setzt sich während der gesamten Schwangerschaft fort. Neue Gehirnzellen entwickeln sich sowohl während der Schwangerschaft als auch im ersten Jahr nach der Geburt.
Fötus: Ab Ende der 8. Woche nach der Befruchtung (man ist 10 Wochen schwanger) bis zur Geburt bezeichnet man den Embryo als Fötus.
Plazenta: ist das Organ, das sich in der Gebärmutter einer schwangeren Frau bildet und den Fötus mit der Mutter verbindet. Auf diese Weise erfolgt die Übertragung von Nährstoffen und Sauerstoff. Sie hilft, die Abfallprodukte aus dem Blut des Kindes zu entfernen und gegen Infektionen zu kämpfen.
Schwangerschaft: Zeitraum zwischen Empfängnis (Konzeption) und Geburt, während sich der Embryo/Fötus im Mutterleib entwickelt.
1. Die Ernährung der Eltern beeinflusst Gesundheit und Wohlbefinden ihrer Kinder
Es ist allgemein bekannt und eine akzeptierte Tatsache unter vielen Laien und Wissenschaftlern, dass Ernährung und Lebensstil einen direkten Einfluss auf die eigene Gesundheit haben. Neue Studien3 zeigen, dass der tatsächliche Gesundheitszustand und das Wohlbefinden einer Person nicht nur von persönlichen Essgewohnheiten und Aktivitäten, sondern auch von folgenden Punkten abhängt:
- Die Umgebung, in der sich die Person im fetalen Stadium entwickelt hat (z.B. Zugang zu Nährstoffen, Hormonhaushalt und Belastungsniveau der Mutter, Plazenta).
- Die Ernährungsform der Eltern.
Mit anderen Worten: Schlechte Lebensgewohnheiten beeinflussen nicht nur jene Personen, die diese leben, sondern auch deren Kinder.
Kurzfristig haben alle diese Veränderungen Einfluss auf die Entwicklung des kindlichen Gehirns, das Wachstum, den Körperbau und den Stoffwechsel. Langfristig beeinträchtigen sie die kognitiven Fähigkeiten des Kindes, die Immunität und das Energieniveau, indem sie die Schulleistungen, das erlernte Bildungsniveau, die Fähigkeit, einen Job auszuüben, sowie die allgemeine Gesundheit beeinflussen.5

Beruhend auf dieser Idee hatte David Barker 1990 das Paradigma der "Developmental Origins of Health and Disease" (DOHaD) entwickelt. Es besagt, dass die Bedingungen vor der Schwangerschaft (Präkonzeption), während der Schwangerschaft und der Laktation die sich entwickelnden Individuen prägen. Dies führt im Fall einer ungünstigen Umgebung zu einer erhöhten Empfänglichkeit für bestimmte Krankheiten im Erwachsenenalter (Prädisposition).1
| Nicht nur Veganer oder Vegetarier sollten das lesen: Veganer essen oft ungesund. Vermeidbare Ernährungsfehler. |
2. Wieso geschieht das?
Schon in den frühesten Entwicklungsstadien (Embryonal-, Fötusstadium) kann der Organismus durch Anpassungen auf zellulärer, molekularer und biochemischer Ebene auf Umwelttrigger (Ursachen oder Auslöser aus der Umwelt) reagieren. Induzieren gewisse ernährungsbedingte Stressoren oder Reize solche Anpassungen, bestehen die Veränderungen im Organismus weiterhin und funktionieren auch in Abwesenheit des Stimulus, der sie initiiert hat.6
Studien bei Tieren folgten zwei Hauptszenarien:
- Überernährung der Mutter – mit hohem Fettanteil, hohem Cholesterin und einer eiweissreichen Ernährung, die zu mütterlicher Fettleibigkeit führen.
- Die Unterernährung der Mutter – durch einen Mangel an Mikronährstoffen (z.B. Ca, Fe, Na, Zn) und Makronährstoffen (z.B. Protein).
Erhielten die Tiere mit einem niedrigen Geburtsgewicht im Erwachsenenalter eine kalorienreiche Ernährung, tendierten sie zu einer erhöhten Fettzunahme. Denn in der fetalen Phase war der Körper darauf programmiert, den Energieaufwand als eine adaptive Antwort auf die Mängel zu beschränken.7
Andere Forschungsergebnisse6 zeigten, dass eine proteinarme Ernährung und eine Kalorienbeschränkung während der Schwangerschaft zu Veränderungen in den Pankreas-Inselzellen / Langerhansschen Inseln führen (z.B. reduzierte Vaskularisation, reduzierte Kapazität zur Erzeugung von Beta-Zellen). Ausserdem rufen sie eine verminderte Empfindlichkeit gegenüber Insulinum in den Muskeln hervor. Auch wenn das Baby nach der Geburt und in der Kindheitsphase eine normale Ernährung erhält, sind die Veränderungen in den Organen irreversibel und erhöhen die Prädisposition für Diabetes oder Stoffwechselerkrankungen.
Das Hauptmerkmal der Zellen während der embryonalen und fetalen Phase ist deren Plastizität (die Fähigkeit der Zellen, sich in andere Zellen zu verwandeln); in derselben Phase entwickeln und strukturieren sich auch die Organe. Deshalb sind Auswirkungen von jeglichen krankheitsfördernden Faktoren in dieser Periode stärker als zu einem späteren Zeitpunkt.
3. Metabolische Ernährungsprogrammierung
Ernährungsprogrammierung oder metabolische Programmierung nennt sich der Prozess der Beeinflussung des Fötus durch Qualität und Quantität der während der Schwangerschaft konsumierten Nährstoffe.
Derzeitige Forschungen und Experimente fanden nur an Tieren (Ratten und Schafen) statt. Dabei hat man die Tiere entweder überfüttert oder bestimmte Nährstoffe verringert, um die Auswirkungen auf ihre Nachkommen zu beobachten. Am Menschen waren nur epidemiologische Studien möglich. Man erkennt jedoch klare Zusammenhänge zwischen den Bedingungen während der Schwangerschaft und den gesundheitlichen Problemen, welche die Menschen später im Erwachsenenleben entwickelt haben.
Warum man bei „Nutritional Programming“ nicht an Menschen experimentiert
"Nutritional Programming" (metabolische Programmierung) erfolgt meist in den Embryonal- und Fötusstadien, wenn die Zellplastizität am höchsten ist. Um embryonale Zellen und die Auswirkungen der Umwelt auf sie zu studieren, müssten Wissenschaftler diese hauptsächlich durch In-vitro-Fertilisation erzeugen, was viele ethische, moralische, religiöse und rechtliche Bedenken auslöst.
Die meisten experimentellen Forschungen an Tieren, die äussere Bedingungen verändern und in weiterer Folge die Auswirkungen auf das neugeborene und erwachsene Tier untersuchen, sind mit Menschen nicht replizierbar.
Gründe, warum man Tierstudien in diesem Bereich immer noch für relevant hält:8
- Ratten, Mäuse und Menschen haben zu 99 % ähnliche Gene.
- Die Umwelt ist einfach zu kontrollieren.
- Der Lebenszyklus ist kurz und die Veränderungen somit nachvollziehbar.
Qualität und Quantität der Nährstoffe, welche die Mutter während der Schwangerschaft konsumiert, können bei den Nachkommen zu signifikanten Veränderungen in Bezug auf die Struktur von Gehirn, Nieren und Herz führen. Dies hängt mit einem erhöhten Risiko für koronare Herzerkrankungen und Störungen der Insulinresistenz zusammen.7
4. Was passiert auf der zellulären Ebene?
Die menschliche Entwicklung im Uterus basiert auf zwei Hauptprozessen: Zellmultiplikation und Zelldifferenzierung (Spezialisierung). Anfänglich gibt es einen kleinen Pool von Zellen (Stammzellen), die sich zu jedem Organ oder Gewebe im Körper entwickeln könnten. Diese Zellen vermehren sich und spezialisieren sich anschliessend auf die Eigenschaften eines speziellen Organs. Der Zeitpunkt, zu dem diese Prozesse stattfinden, unterscheidet sich je nach Organ. Das Herz zum Beispiel formt sich früher als die Geschlechtsorgane und die Lunge entwickelt sich erst in den letzten Wochen der Schwangerschaft.
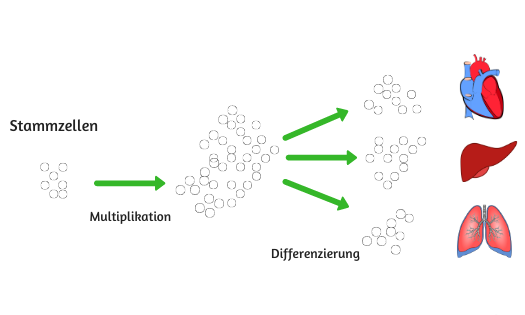
Veränderungen in der Ernährung der Mutter können den Zellteilungs- oder Differenzierungsprozess beeinflussen. Unerwünschte Bedingungen während der Proliferation (Zellteilung) führen z.B. zu einem kleineren Organ, aber mit normalen Zelleigenschaften. Nachteilige Gegebenheiten während der Differenzierung wiederum können zu einem normal grossen Gewebe führen, jedoch mit einer veränderten Form und Funktionalität.7
Ergebnisse verschiedenster Studien zeigen, dass eine schlechte mütterliche Ernährung während der Schwangerschaft meistens zu Veränderungen auf folgenden Ebenen führt:
- Nieren: Tiere, die Nährstoffdefiziten im fetalen Stadium ausgesetzt sind, haben 30-40 % weniger Nephronen (Funktionseinheit der Niere) als der Durchschnitt.7 Studien an Menschen zeigen, dass die australische Aborigine-Population um 20 % häufiger an Nierenversagen leidet als die kaukasische Bevölkerung.9
- Gehirn: Forschungsstudien an Ratten beweisen, dass eine Unterernährung die Dichte der Kapillaren im Gehirn reduziert und dass die für die Appetitkontrolle verantwortliche Dichte der Neuronen geringer ist.10
- Bauchspeicheldrüse: Aufgrund verminderter Ernährungszufuhr haben die Pankreaszellen bei Tieren weniger Langerhanssche Inseln und die Blutversorgung ist reduziert.7
Ist das fetale Wachstum eine zuverlässige Messung für die zukünftige Gesundheit eines Babys?
Bisher war das fetale Wachstum (Gewicht und Grösse) eines der am meisten erforschten Themen, um den Zusammenhang zwischen Umweltbedingungen, Fötusentwicklung und Gesundheitsbedingungen im späteren Leben beweisen zu können.
Die von Barker und seinen Kollegen veröffentlichten Forschungsstudien beruhten auf der Beobachtung von tausenden von Menschen, geboren über einen Zeitraum von zwanzig Jahren. Sie haben folgendes gezeigt: Ein geringes Gewicht bei der Geburt gilt als Vorhersage (Prädiktor) für hohen Blutdruck, ein höheres Blutgerinnungsrisiko, eine beeinträchtigte Glukosetoleranz, Diabetes Typ 2 und das metabolische Syndrom.7
Andere Faktoren, die zukünftige Gesundheitsbedingungen vorhersagen, sind: verminderter Bauchumfang, grosser Kopfumfang in Bezug auf die Körperlänge und geringes Gewicht im Verhältnis zur Körperlänge.
Die Forschungsstudie von Rosenboom11 über die niederländische Hungersnot und ihre Auswirkungen auf die in dieser Zeit geborenen Kinder zeigt deutlich, dass eine Mangelernährung während der Schwangerschaft die Gesundheit dieser Personen im späteren Leben beeinflusst.
Tierforschungen beweisen, dass die Auswirkungen der Umweltbedingungen über das fetale Wachstum hinausgehen. Aber da dies weniger offensichtlich ist und sich auf verschiedenen Ebenen ausdrückt, ist es schwieriger, es experimentell zu beobachten.
Auch wenn der Fötus normal weiterwächst, kann das Nährstoffdefizit einen gravierenden Einfluss auf die zukünftige Gesundheit haben. Aus dieser Perspektive kann das Geburtsgewicht nicht nur der einzige Gesundheits-Prädiktor für das Erwachsenenleben sein.
Nach der Beobachtung der Kinder, die während und nach der niederländischen Hungersnot zur Welt kamen, stellte Rosenboom fest, dass eine mütterliche Unterernährung während der Schwangerschaft die Gesundheit dauerhaft beeinflussen kann, auch ohne die Grösse des Babys bei der Geburt zu beeinträchtigen.10 Darüber hinaus hängen die Auswirkungen der Unterernährung vom Zeitpunkt der Schwangerschaft und dem kritischen Zeitfenster der Entwicklung der Organe und der Systeme ab.
Zum Beispiel hatten jene Individuen, deren Mütter vor der holländischen Hungersnot schwanger waren und in der späteren Schwangerschaft einer energiearmen Umgebung ausgesetzt waren, als Erwachsene ein erhöhtes Risiko für Insulinresistenz und beeinträchtigte Glukosetoleranz. Diejenigen, deren Mütter während der Hungersnot schwanger gingen, hatten während des Erwachsenenalters ein erhöhtes Risiko für einen hohen Cholesterinspiegel und koronare Herzkrankheiten.11
Variationen in der mütterlichen Ernährung sind die besten Einflusswerte (Prädiktoren) für fetale Veränderungen und auch der stärkste Antrieb für die „fetale Programmierung“. Allerdings gibt es viele andere Faktoren, die gleichzeitig den Ernährungsstatus des Fötus beeinflussen: die körperliche Verfassung der Mutter, das Alter, die körperliche Aktivität, der Blutfluss zur Plazenta, die Effizienz des Nährstofftransfers, die hormonelle Balance der Mutter usw.
5. Epigenetik ist der Hauptprozess der "Ernährungsprogrammierung"
Die Ernährung der Mutter beeinflusst sowohl die Entwicklung des Fötus (Veränderungen bei der Zellteilung und Differenzierung) als auch dessen Genexpression (epigenetische Prozesse).
Wie Epigenetik funktioniert
Stellen Sie sich den menschlichen Organismus als riesige, komplexe Fabrik vor, wobei die Körperzellen die grundlegenden Arbeitseinheiten sind. Um zu wissen, wie alles funktioniert, benötigen Zellen Informationen, grundlegende Regeln und Abläufe. Diese riesige Datenbank von Regeln und Abläufen befindet sich in der DNA, sorgfältig organisiert in bestimmten Informationssequenzen namens Gene. Es gibt über 20'000 Gene und jede Zelle hat auf alle Zugriff, aber nicht jede Information ist "gelesen" und umgesetzt (implementiert). Die Informationen lassen sich nach weiteren Anweisungen, den sogenannten epigenetischen Markern, selektiv aufrufen und anwenden. Alle diese epigenetischen Marker bilden zusammen das Epigenom, das für jeden Menschen unverwechselbar ist und stark von Umwelteinflüssen abhängt. Lesen Sie hier mehr über den Unterschied zwischen Genetik und Epigenetik.
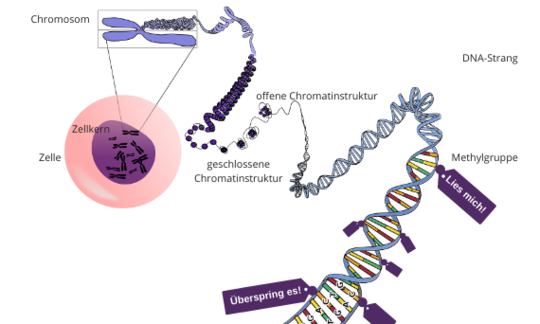
Epigenetik (wörtlich "Übergenetik") ist der Prozess einer Hervorhebung oder Definition bestimmter Teile dieser Regeln und Abläufe. "Aktive" Abschnitte sind sichtbar und befehlen den Zellen, sie zu beachten und zu exprimieren. Andere epigenetische Faktoren schalten bestimmte Gene ab und machen sie unzugänglich, sodass die Zellen diese Informationen nicht lesen und anwenden können.
Hauptmechanismen epigenetischer Veränderungen
Die an epigenetischen Veränderungen beteiligten Hauptmechanismen sind:12
- Methylierung: eine Methylgruppe (chemische Verbindung), die an die DNA gebunden ist und die Funktion eines spezifischen Gens modifiziert.
- Histonmodifikation: Weil die DNA sehr lang ist, muss der DNA-Strang um Proteinstrukturen, "Histone", gewickelt sein. Auf diese Weise bildet sie eine Chromatinstruktur. Ist sie zu eng gewickelt, kann die Zelle die Informationen in dieser Sequenz nicht lesen. Sind die Bindungen zwischen diesen Histonen locker, lassen sich die Informationen lesen und anwenden.
Bei einem Experiment erhielten Tiere eine Diät, bei der Methylgruppen, Folsäure, Vitamin B12 und Methionin fehlten (für einen Zeitraum von 8 Wochen vor der Empfängnis und für die ersten 6 Tage der Schwangerschaft). Männliche Nachkommen aus diesen Mutterschafen waren insulinresistent und hatten einen erhöhten Blutdruck.13
Dieses Phänomen ist am sichtbarsten bei eineiigen Zwillingen, die ihr Leben in verschiedenen Umgebungen verbringen. Auch wenn das Genom (alle erblichen Informationen) dasselbe ist, haben diese beiden Menschen eine andere Körperfunktionalität und andere gesundheitsbezogene Ergebnisse.
Epigenetik – das Gute und das Schlechte
Die Rolle der Epigenetik besteht darin, dem Körper zu helfen, grosse Veränderungen in der Umwelt und im Leben zu bewältigen. Zum Beispiel hilft sie dem Organismus, während Hungersnöten zu überleben, den weiblichen Körper während der Schwangerschaft oder den Körper von Jugendlichen in der Pubertät zu verändern.
Probleme treten auf, wenn diese epigenetischen Veränderungen beginnen, Krankheiten zu erzeugen. Manchmal sind die aktiv gemachten Gene mit bestimmten Krankheiten assoziiert. Krebs könnte zum Beispiel durch das Aktivieren von zu vielen wachstumsfördernden Genen - oder im Gegenteil durch das Ausschalten von tumorunterdrückenden Genen - entstehen.
Epigenetische Veränderungen sind vererbbar
Es ist eine wichtige Tatsache, dass diese epigenetischen Marker nicht fixiert sind. Sie sind während des gesamten Lebens veränderbar, z.B. unter dem Einfluss von Ernährung und Umwelt. Einige können sogar von früheren Generationen her vererbt sein und lassen sich weiter übertragen.
In einem Experiment des Zentrums für Reproduktionsbiologie an der Washington State University setzte man schwangere Ratten relativ hohen Mengen an Methoxychlor (Insektizid) und Vinclozolin (Fungizid) aus. Infolgedessen wiesen männliche Nachkommen eine verminderte Spermienproduktion und eine erhöhte Unfruchtbarkeit auf. Die Forschungsstudie zeigte, dass die Ursache dieser Manifestationen ein Methylierungsprozess war, der zwei Gene beeinflusste. Die nächsten vier Generationen beobachtete man ohne Verabreichung von Pestizid-Substanzen. 90 % der männlichen Ratten zeigten die gleichen negativen Auswirkungen.14
Studien von Dr. Erica Watson an der Universität von Cambridge dokumentieren: Weisen entweder die mütterliche Grossmutter oder der mütterliche Grossvater eine spezifische genetische Mutation auf (bekannt als Mtrr-Mutation), die einen Folsäure-Mangel verursacht, sind ihre genetisch normalen Enkel, welche die genetische Mutation nicht geerbt haben, noch immer dem Risiko bestimmter Entwicklungsstörungen ausgesetzt.16
6. Wie Ihr Lebensstil die Gesundheit Ihrer Kinder beeinflussen kann
Für lange Zeit hielten Wissenschaftler daran fest, dass sich Unterernährung und westliche Krankheiten gegenseitig ausschliessen. Überraschenderweise zeigen Experimente mit Einschränkung der Ernährungszufuhr bei schwangeren Tieren die gleichen Ergebnisse bei den Nachkommen wie Experimente, bei denen die Tiere überernährt waren: hoher Blutdruck, Glukoseintoleranz, Insulinresistenz und eine grössere Prädisposition gegenüber Fettleibigkeit.17
Hier sind die wichtigsten Auswirkungen der elterlichen Ernährung, des Gewichts und des Lebensstils der Eltern (vor und nach der Empfängnis) auf ihre Nachkommen:
| Elterliche Ernährung und Lebensstil | Möglicher Einfluss auf die Kinder |
| fettlastige Ernährung | erhöhter Blutdruck, vaskuläre Erkrankung (endotheliale Dysfunktion)18 |
| eiweisslastige Ernährung | Veränderung des Energieverbrauchs, Fettleibigkeit19 |
| hohe Cholesterinwerte der Mutter in der Frühschwangerschaft | Übergewicht / Fettleibigkeit, erhöhter Körperfettanteil, erhöhter Cholesterinspiegel mit ca. 4 Jahren23 |
| Unterernährung der Mutter während der Schwangerschaft | erhöhte Glukoseproduktion in der Leber, gestörte Fettsäurenoxidation, Ketose-Resistenz, Veränderungen der Glukoseaufnahme2 |
| mütterliche Überernährung | Fettleibigkeit, Glukoseintoleranz, veränderte Appetitregulierung im Gehirn |
| proteinarme Ernährung | Die Expression von 102 Genen im Hypothalamus und 36 Genen in den Nieren ist modifiziert.20 |
| mütterliche Fettleibigkeit vor und während der Schwangerschaft und hoher Leptinspiegel (wegen Fettleibigkeit) | Hohe Leptinspiegel während der Entwicklung des Hypothalamus beim Fötus führen zu Leptinresistenz, Hyperphagie und verminderter Fähigkeit des Kindes, den Appetit zu regulieren.21 höherer Blutdruck, grössere Neigung zu Fettleibigkeit und Insulinresistenz.1 |
| Übergewicht vor der Schwangerschaft | erhöhter Körperfettanteil und erhöhter systolischer Blutdruck beim künftigen Kind22 |
| eisenarme Ernährung der Mutter vor und während der Schwangerschaft | Veränderungen der Herzentwicklung während der fetalen Phase, die zu erhöhtem Blutdruck und Veränderungen des Fettsäurestoffwechsels führen können7 |
| Vater beginnt früh zu rauchen | erhöhter Body-Mass-Index bei Söhnen23 |
| Alkoholkonsum des Vaters vor der Empfängnis | niedrigeres Geburtsgewicht, Entwicklungsverzögerung, beeinträchtigte Immunität, Verhaltensdefizite, Hyperaktivität und verminderte Leistungsfähigkeit24 |
Der Schweregrad dieser Effekte hängt mit der Dauer der Exposition und der Menge der Schadstoffe zusammen - sowie mit der Entwicklungsperiode, in welcher der schädliche Einfluss auftritt.
Bis vor kurzem waren Wissenschaftler der Ansicht, dass epigenetische Marker, welche die Gene des Fötus beeinflussen, eine dauerhafte Wirkung auf seine Gesundheit und sein Wohlbefinden haben. Neue Forschungen untersuchen, ob diese epigenetischen Marker auch im Erwachsenenalter flexibel bleiben. Dies wäre positiv, wenn sich die Umgebungsbedingungen günstig verändern.
Jede Person trägt die Verantwortung für seine eigenen Gene, Gottfried Schatz
Mit anderen Worten, auch wenn gewisse epigenetische Modifikationen während des fetalen Stadiums stattfanden und im Erwachsenenalter zu gesundheitlichen Einschränkungen führen, wäre es möglich, diese Wirkung im Erwachsenenalter abzuschwächen oder umzukehren. Der ständige Kontakt mit positiven Umgebungsreizen (z.B. gesunde Ernährung und Lebensstil, positive Emotionen) könnte die Aktivierung oder Abschaltung der Gene verändern, chronische Krankheiten wie Krebs, Diabetes, Bluthochdruck und Herzprobleme verhindern oder umkehren.
Die meisten dieser Erkenntnisse sind immer noch sehr spekulativ. Jedoch gibt es eine steigende Anzahl an Forschungen über epigenetische Modifikationen und Ernährungs-Programmierung, die untersuchen, welche Auswirkungen die Ernährung der Eltern und ihre Entscheidungen bezüglich Lebensstil auf ihre Kinder haben.
Literatur
24 Quellenangaben
- Tarrade A, Panchenko P, Junien C, Gabory A. Placental contribution to nutritional programming of health and diseases: epigenetics and sexual dimorphism. Journal of Experimental Biology 2015.
- Martínez JA, Cordero P, Campión J, Milagro FI. Interplay of early life nutritional programming on obesity, inflammation and epigenetic outcomes. Proc Nutr Soc. 2012 May;71(2):276-83.
- Wadhwa PD, Buss C, Entringer S, Swanson JM. Developmental Origins of Health and Disease: Brief History of the Approach and Current Focus on Epigenetic Mechanisms. Seminars in reproductive medicine. 2009;27(5):358-368. doi:10.1055/s-0029-1237424.
- Vickers, MV. Early Life Nutrition, Epigenetics and Programming of Later Life Disease. Nutrients 2014.
- Uauy R, Kain J, Corvalan C. How can the Developmental Origins of Health and Disease (DOHaD) hypothesis contribute to improving health in developing countries? The American journal of clinical nutrition. 2011.
- Patel MS, Srinivasan M. Metabolic Programming: Causes and Consequences. The Journal of Biological Chemistry, January 2011; 277.
- Langley-Evans SC. Nutritional programming of disease: unravelling the mechanism. Journal of Anatomy. 2009;215(1):36-51.
- Gunter C, Dhand R. Human biology by proxy. Nature 420, 509, 5 December 2002.
- Singh GR, Hoy WE. Kidney volume, blood pressure, and albuminuria: findings in an Australian aboriginal community. J Kidney Dis. 2004.
- Plagemann A, Harder T, Rake A, et all. Hypothalamic nuclei are malformed in weanling offspring of low protein malnourished rat dams. J Nutr. 2000.
- Roseboom TJ, van der Meulen JH, Ravelli AC, et all. Effects of prenatal exposure to the Dutch famine on adult disease in later life: an overview. Mol Cell Endocrinol. 2001.
- Kanherkar RR, Bhatia-Dey N, Csoka AB. Epigenetics across the human lifespan. Front Cell Dev Biol. 2014; 2: 49.
- Sinclair KD, Allegrucci C, Singh R, et al. DNA methylation, "insulinresistance", and blood pressure in offspring determined by maternal periconceptional B vitamin and methionine status. Proc Natl Acad Sci USA. 2007;104:19351–19356.
- Weinhold B. Epigenetics: The Science of Change. Environmental Health Perspectives. 2006.
- Anway MD1, Cupp AS, Uzumcu M, Skinner MK. Epigenetic transgenerational actions of endocrine disruptors and male fertility. Science. 2005 Jun 3;308(5727):1466-9.
- Padmanabhan N, Jia D, Geary-Joo C, Wu , Ferguson-Smith AC, Fung E. et all. Mutation in Folate Metabolism Causes Epigenetic Instability and Transgenerational Effects on Development. J. Cell, 2013 Sept. 2.
- Langley-Evans SC. Developmental programming of health and disease. Proc Nutr Soc. 2006.
- Khan IY, Taylor PD, Dekou V et all. Gender-linked hypertension in offspring of lard-fed pregnant rats. Hypertension. 2003.
- Daenzer M, Ortmann S, Klaus S, Metges CC. Prenatal high protein exposure decreases energy expenditure and increases adiposity in young rats. J Nutr. 2002.
- Langley-Evans SC, Bellinger L, McMullen S. Animal models of programming: early life influences on appetite and feeding behaviour. Matern Child Nutr. 2005.
- Samuelsson AM, Matthews PA, Argenton M, Christie MR, McConnell JM, Jansen EHJM et all. Diet-Induced Obesity in Female Mice Leads to Offspring Hyperphagia, Adiposity, Hypertension, and "InsulinResistance". A Novel Murine Model of Developmental Programming. Hypertension. 2008;51:383-392.
- Daraki V, Georgiou V, Chalkiadaki G, Karachaliou M, Koinaki S. Metabolic dysregulation in early pregnancy in association with offspring cardiometabolic risk in preschool children. Program of prevention and early diagnostic of obesity and neurodevelopment disorders in preschool age children, Crete, Greece, NSRF 2007-2013 project, MIS 349580.
- Pembrey ME, Bygren LO, Kaati G, Edvinsson S, Northstone K, Sjöström M, Golding J, ALSPAC Study Team. Sex-specific, male-line transgenerational responses in humans. Eur J Hum Genet. 2006 Feb; 14(2):159-66.
- Curley JP, Mashoodh R, Champagne FA. Epigenetics and the Origins of Paternal Effects. Hormones and behavior. 2011;59(3):306-314.

Kommentare