Reseña de «Medicina mortal y crimen organizado», Gøtzsche
El profesor Gøtzsche, investigador médico danés, expone con ejemplos y estudios científicos cómo la industria farmacéutica corrompe nuestra sanidad.

Tabla de contenido
- Conclusión
- 1. Resumen
- 2. Reseña del libro
- 2.1. Confesiones desde dentro
- 2.2. El crimen organizado como modelo de negocio de las grandes farmacéuticas
- 2.3. Muy pocos pacientes se benefician de los medicamentos
- 2.4. Estudios clínicos: un contrato social con los pacientes roto
- 2.5. Conflictos de intereses en las revistas médicas
- 2.6. El poder corruptor del dinero fácil
- 2.7. ¿Qué hacen miles de médicos con el dinero que reciben de la industria?
- 2.8. Estrategias de ventas agresivas
- 2.9. Supervisión de los medicamentos inadecuada
- 2.10. Acceso público a los datos de las autoridades competentes
- 2.11. "Neuront..": medicamento antiepiléptico y antitodo
- 2.12. Merck, donde los pacientes mueren primero
- 2.13. El fraudulento estudio del "Celecox.." y otras mentiras
- 2.14. Medicamentos costosos para sustituir los baratos prescritos a los pacientes
- 2.15. Todo perfecto con los niveles de azúcar en sangre, pero el paciente muere
- 2.16. La psiquiatría, el paraíso de la industria farmacéutica
- 2.17. Empujar a los niños al suicido con pastillas para la felicidad
- 2.18. Intimidación, amenazas y violencia para mejorar las ventas
- 2.19. Los cuentos chinos de la industria, al descubierto
- 2.20. El fracaso del sistema pide una revolución
- 2.21. El que ríe el último...
- 3. Sobre el libro
Conclusión
Obtuvimos de una empresa mundial, la demanda de 4864 nombres diferentes para no usar. Existen principalmente medicamentos recetados, etc. Incluyendo "I" para el ingrediente activo en el cuerpo que inhibe la diabetes. Ahora usamos "accesos directos" y hemos eliminado algunos pasajes y numerosos enlaces útiles. La contribución original solo puede ser vista por los miembros (la membresía es posible en la parte superior izquierda de nuestras páginas, EA 30/05/19).
**************
El profesor y doctor en medicina Peter Christian Gøtzsche describe de forma precisa y detallada los chanchullos (cabales) de la industria farmacéutica, que van desde fraudes, ocultación de estudios negativos, cohecho, intimidación a amenazas a críticos (crítica), entre otros.
A pesar de todo, en el libro no se critica el sistema capitalista; es una lectura ligera que casi parece una novela negra. En esta reseña solo podemos exponer los hechos de manera concisa. Faltarán los numerosos ejemplos con información concreta.
El autor aporta una serie de soluciones que resume en el capítulo 21 del libro. Palabras clave: laboratorios independientes y agencias reguladoras, rechazo de dinero y beneficios de la industria para todos aquellos involucrados en temas de salud, es decir, personal médico, hospitales, universidades, institutos, grupos de autoayuda, revistas, periodistas, políticos, etcétera, así como la prevención de los conflictos de intereses entre los expertos.
El libro es de lectura obligatoria para todos aquellos médicos que crean que la industria farmacéutica se centra en los pacientes y no trabaja para su propio beneficio. ¿Debería recomendarse a los legos que no cuenten con información previa?
No interrumpa ningún tratamiento tras leer el libro, pero no está de más consultar con el personal médico e, incluso, recomendarles que le echen un vistazo ellos mismos. Un enlace basta. Hay medicamentos vitales.
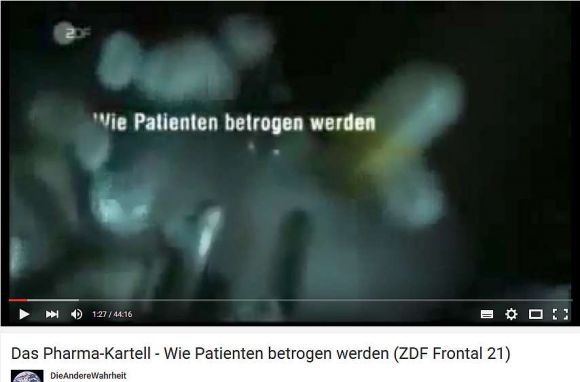
En contraste con este libro, debería saberse también que la esperanza de vida actual también se la debemos a la industria farmacéutica. Esta crítica abrumadora, pero objetiva no pretende transmitir eso. Que Gøtzsche (escrito en alemán Goetzsche) tiene razón lo confirman diferentes medios. Por ejemplo, la cadena ZDF alemana o algunos vídeos en Youtube. Si pincha sobre las imágenes, se le redirigirá al vídeo.
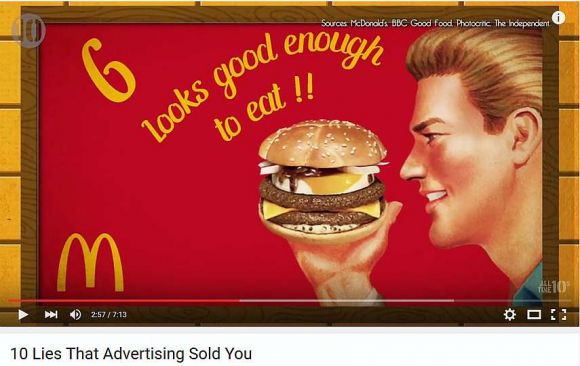
 | Video: Ein Pharma-Insider packt aus (Una persona de dentro de la industria revela la impactante realidad), 3:28 min. Del canal de YouTube DieAndereWahrheit (La otra verdad). |
La cadena de televisión alemana ZDF destaca por sus rigurosos documentales. Este, por ejemplo, demuestra que el libro en cuestión no exagera en absoluto.
1. Resumen
¿De qué trata este libro? Expone los métodos que emplean los grupos farmacéuticos y sus administradores, cuyo objetivo es aumentar las ganancias a cualquier precio. Según el autor, podrían hacer lo correcto sin necesidad de trucos, es decir, ofrecer medicamentos efectivos, sin efectos secundarios y económicos. Pero hoy en día este no puede ser el objetivo de una empresa que quiera tener éxito en el sector. La sociedad debe cambiar.
El autor dedica el libro a las muchas personas honestas que hay en la industria farmacéutica que están igual de indignados que en él por los tratos criminales de sus superiores y las consecuencias que estos tienen en los pacientes y en la economía.
En el caso de los grupos que se dedican a la industria de la nutrición sucede algo parecido, como ya destacamos en esta reseña del libro «Sal, azúcar, grasas» de Michael Moss. Por este libro, Michael Moss recibió el premio Pulitzer.
Cómo se comportan las personas cuando hay dinero o prestigio en juego
Ambos libros, «Sal, azúcar, grasas» y «Medicinas que matan» no hacen sino mostrar cómo se comportan las personas cuando hay dinero o prestigio en juego.
Fallamos al transmitir, ya desde niños, qué es la ética y lo que esta significa. La profundización, es decir, la ética aplicada (véase el apartado de «Información» dentro de la página) y la filosofía deberían enseñarse a los jóvenes adultos de forma obligatoria y sin importar el género. De otra manera, no hay posibilidad de que la sociedad cambie, pues es esta la que debe cambiar y no el resto. Es algo similar a lo que sucede cuando tratamos de introducir la democracia que tenemos en los países occidentales en un pueblo que no conoce el concepto.
En Wikipedia podemos encontrar información sobre la ética de los negocios tanto en español como en inglés. Algunos de los valores centrales son la humanidad, la solidaridad o la responsabilidad, y sobre todos ellos se puede leer.
Si se compara la teoría con la práctica, con los enredos de la política, solo se puede deducir que las sugerencias bien intencionadas y correctas del autor no son realistas, pues están resumidas de forma muy breve. Falta incluir la voluntad de las bases para cambiar ese estado. Por ahora, las bases están lejos de tratar el problema o siquiera de entenderlo, y lo mismo con sus implicaciones a largo plazo.
 |
|
Aquí encontrará la declaración CONSORT 2010 traducida al castellano.
 | Video: Martin Sonneborn entrevista a un representante de ProGenerika. (3:42 min., de QVCinsider, extraído del programa Heute-Show, de la cadena alemana ZDF, 14.5.2010) |
Este fragmento de Youtube trata sobre medicamentos baratos procedentes de China o la India. Es gracioso, pero no aporta nada al libro.
¿Qué pasó tras la emisión de ese programa? ¿Era todo un montaje? ¡No!
Cuando uno ve este vídeo le asaltan las dudas. Martin Sonneborn, reportero satírico de la ZDF, creó tal situación que cuesta creer que algo así sea real cuando se trata con el brazo astuto y financieramente potente de la industria farmacéutica.
Yo tampoco me lo podía creer y hoy la reacción del representante de las farmacéuticas Peter Schmidt me da verdadera lástima. Me dio casi vergüenza ajena... Llegué a pensar, simplemente: «Esto no puede ser verdad». Especialmente con los dos «confidentes» que aportó el programa y también con el cartel que el señor Sonneborn tenía pegado en la espalda y que solo los espectadores podíamos ver.
Pero hubo un reportaje el 22 de julio de 2010 titulado «Martin Sonneborg im Gespräch» (Charla con Martin Sonneborg) para el periódico alemán Süddeutschen Zeitung (que se puede leer todavía en su página web, sueddeutsche.de) con el título de «Martin Sonneborn im Gespräch, Todesurrteil» (Charla con Martin Sonneborg, sentencia de muerte) en la web.
El reportaje se titula «Ein Todesurteil gegen mich», es decir «Mi sentencia de muerte» con el siguiente subtítulo: «¿Payaso político, periodista de guerrilla o estafador de etiqueta? Martin Sonneborg sobre Guido Westerwelle, el ingenuo representante de la industria farmacéutica y las acusaciones de la ZDF contra el humorista satírico». Una entrevista de Antje Hildebrandt.
Es bien sabido que a Martin Sonneborn, que en aquel momento tenía 45 años, le encantaba dejar en evidencia a políticos y ciudadanos de a pie.
Sin embargo, ni él ni Peter Schmidt recibieron una palmadita en la espalda tras la entrevista. A continuación, una cita traducida del artículo en alemán del Süddeutsche Zeitung:Entretanto, el representante farmacéutico Peter Schmidt ha sido despedido, entre otras cosas, por afirmar que las pastillas fabricadas en oriente, mucho más baratas, son igual de efectivas que las alemanas. ¿Le dio pena?
Y la respuesta del señor Sonneborn: Sí, Peter Schmidt me cayó bien. Me dio pena que la entrevista terminase con su despido. Por otro lado, en mi opinión, a los representantes se les permite todo. Antes de ser secretario general del grupo "ProGenerika", valorado en miles de millones de euros, Schmidt fue miembro del grupo de trabajo “Salud y seguridad social” del grupo parlamentario SPD. Y con nuestro reportaje queríamos poner de manifiesto esa relación que existe entre la clase política y los grupos de presión.
Prólogo y opiniones
El profesor y doctor Gerd Gigerenzer, psicólogo y director del Max-Planck-Institut für Bildungsforschung, alaba el libro y dice de él que le ha abierto los ojos.
El profesor y doctor en medicina Peter Sawicki (enlace en alemán) diabetólogo, coincide con el autor en que:
El doctor Sawicki fue director del Institut für Qualität und Wissenschaftlichkeit im Gesundheitswesen (IQWIG) (enlace en alemán). ¡La política le llamó en el año 2010!
El doctor en medicina y farmacología Wolfgang Becker-Brüser (enlace en alemán), además de editor de la publicación médica alemana Arznei-Telegramm (enlace en alemán), declara que el provocativo título no exagera en absoluto. La institución responsable de dicha publicación médica, que no cuenta con publicidad, es la A.T.I. Arzneimittelinformation Berlin GmbH.
El exitoso escritor y doctor en filosofía Frank Wittig considera al autor como el mejor cazador de mafiosos farmacéuticos de todo el mundo. El mismo doctor Wittig publicó el libro «Die Weisse Mafia» (La mafia blanca) en febrero de 2013, con el que consiguió entrar en la lista de los más vendidos del periódico alemán Der Spiegel. Wittig también publicó otro libro, «Krank durch Früherkennung» (Enfermo por un diagnóstico precoz) en septiembre de 2015. A continuación puede echar un vistazo a la entrevista que realizó a través de la editorial Thieme y que lleva por título Mafiöse Machenschaften (Chanchullos mafiosos), así como la entrevista que le hicieron en la radio alemana SWR1 sobre el libro publicado por la editorial Riba en el que habla de las pruebas sinsentido para la prevención del cáncer de mama y de próstata.
En su prólogo, el profesor y doctor en medicina Richard Smith (enlace en inglés) alaba la forma en que Gøtzsche desenmascara sin concesiones los métodos que utilizan las corporaciones farmacéuticas y sus secuaces.
El doctor Smith trabajó para el British Medical Journal (BMJ) durante 25 años, 13 de ellos como editor.
Wikipedia, sobre el doctor Smith: pertenece a la Junta de directores de la Public Library of Science, un editor de investigaciones científicas y médicas de libre acceso. Fue editor jefe de Cases Journal (enlace en inglés), también de libre acceso, cuyo objetivo es recopilar casos clínicos.
Asimismo, también fue director de UnitedHealth Europe, uno de los departamentos de UnitedHealth.
Véase también los libros: «El jardinero fiel» (The Constant Gardener) de John le Carré, publicado en 2001, y la película homónima de Fernando Mirelles del año 2005.
Smith cita a un exvicepresidente de Pfitzer de esta manera:
Las similitudes entre esta industria y el crimen organizado son aterradoras. La mafia gana una cantidad escandalosa de dinero. Y la industria también. Los efectos secundarios del crimen organizado son muertes y asesinatos. Y los de esta industria también. La mafia cautiva a políticos y ciudadanos. Y los grupos farmacéuticos también. (pág. 13)
En otro prólogo, el profesor y doctor en medicina Drummond Rennie (enlace en inglés), exeditor adjunto de la publicación médica Journal of the American Medical Association (Revista de la Asociación Médica Estadounidense) destaca las capacidades científicas únicas del autor, sus investigaciones, su integridad, su veracidad y su coraje. Dado que él también ha recopilado numerosas experiencias con la industria farmacéutica a lo largo de las décadas y que conoce bien al doctor Gøtzsche, afirma que confía en la exactitud de la información que este aporta. El título de su prólogo reza: Indignación basada en la evidencia.
2. Reseña del libro
El profesor y doctor en medicina Peter Christian Gøtzsche expone que las principales epidemias están controladas en la mayoría de los países, pero critica que, a pesar de todo, muchas personas pobres mueren debido al sida o a la malaria, pues no pueden permitirse unos medicamentos tan caros. Ahora hay dos nuevas epidemias: el tabaco y los medicamentos.
En Estados Unidos y Europa, los medicamentos son la tercera causa de muerte, solo por detrás de las enfermedades coronarias y del cáncer. (pág. 23)
Gøtzsche compara a la industria tabacalera con la farmacéutica: aunque se hayan realizado estudios sobre el tabaquismo activo y pasivo y su adicción, estos no se han publicado y su existencia se ha mantenido en secreto. Los estudios proceden, en parte, de la misma Philip Morris, la gran tabacalera.
Esto es corrupción
Cuando algún científico reconocido afirma que un producto es peligroso, enseguida aparecen estudios que demuestran lo contrario para desestabilizar a los ciudadanos. De esta manera, la industria—tanto la tabacalera como la farmacéutica— gana tiempo. Esto es corrupción.
(pág. 24)

Hay distintos tipos de adicciones: drogodependencia con sustancias psicotrópicas, que pertenece a un grupo de desórdenes psicológicos (síndrome) y del comportamiento debido al consumo reiterado de psicoactivos. Es habitual un deseo por la sustancia fuerte, ya sea de forma periódica o habitual, acompañado de dejadez en cuanto a responsabilidades o actividades, pérdida de control (enlace en alemán) y un consumo compulsivo de la sustancia. En medicina, esto se conoce como adicción.
Sin embargo, hay ciertas formas de adicción que la sociedad suele tolerar como el tabaquismo, la adicción a los videojuegos, la ludopatía, la adicción a la cafeína o el alcoholismo. Eche un vistazo también a los peligros de ser un fumador pasivo.
Pocas personas saben que la cafeína puede tener efectos tóxicos si se consume más de un gramo al día. Un gramo de cafeína se corresponde a la cantidad que encontramos en 10 litros de un refresco comercial o en 12 latas de 250 mililitros de una bebida energética.
En el siguiente enlace, Wikipedia expone el potencial adictivo de diferentes sustancias. Es interesante saber que: «Las sustancias con mayor potencial adictivo son la heroína y la nicotina». Pinche aquí para saber más sobre la heroína y la nicotina.
En Estados Unidos, las anuncios de televisión animan a los espectadores a tomar «píldoras», es decir, comprimidos o cápsulas, para volver a tomar las riendas de su vida. Igual que los personajes de la novela de Aldous Huxley «Un mundo feliz» (1932) tomaban todos los días pastillas de "som.".
¿Por qué lo hacemos? En palabras del autor, esto se debe a que las empresas farmacéuticas venden mentiras en lugar de medicamentos (pág. 25)
En este libro no se trata el éxito en la lucha contra las infecciones, algunos tipos de cánceres o trastornos metabólicos como la diabetes de tipo uno, sino del fracaso del sistema y de sus causas. El autor menciona:
La literatura científica sobre medicamentos se ve distorsionada con estudios que tienen fallos de diseño y a los que se les realizan análisis defectuosos, así como con la publicación selectiva de estudios y de datos, la supresión de los resultados no deseados y el uso de escritores fantasma en la publicación de artículos.
Consideramos escritores fantasma a aquellos que se mantienen en el anonimato. Los artículos se publican con el nombre de profesores reputados, aunque a menudo no hayan tenido nada que ver con el texto. (pág. 26)
2.1. Confesiones desde dentro
El autor explica sus primeras experiencias con medicamentos preventivos.
Algunos complementos vitamínicos pueden reducir la esperanza de vida
Complementos vitamínicos con ocho años. En los años cincuenta, la gente todavía creía en los grandes beneficios de tomar vitaminas porque sí.
No fue hasta 2008 que apareció un estudio en el que se afirmaba que algunos de estos complementos podían reducir la esperanza de vida.
Véase Bjelakovic G, Nikolova G. et al.: «Antioxidant supplements for prevention of mortality in healthy participants and patients with various diseases». Cochrane Database Syst Rev.
El entero-vioformo para prevenir las diarreas puede causar daños nerviosos, parálisis y trastornos en la vista
Su segunda experiencia al respecto fue con el entero-vioformo (Clioquinol) para prevenir las diarreas en Italia. Esta decisión fue un sinsentido, pues el medicamento solo era eficaz contra las infecciones protozoarias (amebas) o contra las shigella, de las cuales no había posibilidad de contagiarse en Italia.
Sin embargo, si este medicamento se consumía durante un periodo de tiempo largo, podía provocar daños nerviosos, parálisis en las piernas e, incluso, problemas graves de visión.
La empresa Ciba (hoy parte de Novartis) lo sabía desde hacía bastante tiempo. Para 1970, 10 000 personas padecían neuropatía mielo-óptica subaguda (enlace en inglés), por la que la empresa tuvo que compensarles con 490 millones de dólares. Pese a ello, no retiraron el medicamento del mercado hasta 1985. En algunos idiomas, la neuropatía mielo-óptica subaguda también se denomina SMON, por el acrónimo en inglés.
Tras terminar su carrera en química y biología, el autor comenzó a trabajar para la empresa Astra (hoy en día, AstraZeneca) como representante. Allí aprendió a convencer a los médicos para que escogieran el producto de la empresa y no el de la competencia y a que pidiesen la mayor cantidad posible.
Medicamentos milagrosos
En los años 60 aparecieron los corticoides como remedio milagroso para tratar la artritis reumatoide. Los graves efectos secundarios (p.ej., fracturas en los huesos) no se descubrieron hasta años más tarde.
En aquel momento, acababa de introducirse la Globacilina, una penicilina que, en teoría, era muy superior a los medicamentos de la competencia, para tratar la rinosinusitis aguda. Sin embargo, los datos que se aportaron eran falsos.
Esto afectó a la autoestima del autor, sobre todo después de leer el libro «Muerte de un viajante» (1949) de Arthur Miller (1915-2005).
Otro «remedio milagroso» fueron los comprimidos de zinc para las úlceras venosas. A pesar de los impresionantes estudios realizados por la empresa, el análisis posterior del grupo Cochrane reveló que estos no tenían ningún efecto beneficioso.
Ocho meses después, le ascendieron a jefe de producto. Como tal, era responsable de la venta del espray para el asma "Brican.." (terbutalina, inhalador). El objetivo era conseguir que los médicos prescribiesen a sus pacientes la inhalación regular del espray. El número de muertes en personas asmáticas también aumentó.
Asma
El profesor, doctor y epidemiólogo Neil Pearce, de la London School of Hygiene & Tropical Medicine (LSHTM), y antiguo presidente de la Asociación Internacional de Epidemiología (IEA, por sus siglas en inglés), escribió un artículo sobre el poder de la industria farmacéutica y sus aliados médicos a sueldo.
Lo que escribe sobre el tratamiento de los asmáticos es inquietante. (pág. 39)
Hoy en día ya no se recomienda la inhalación regular de los llamados beta-miméticos de acción inmediata (beta-2-simpaticomiméticos) (enlace en alemán). Como resultado, el número de fallecimientos entre las personas asmáticas se ha reducido.
Además, se intentó utilizar la tertabutalina en casos de bronquitis crónica, pero no llegó a aprobarse, ya que no contaba con estudios que lo respaldaran. Otra aplicación teórica del medicamento era como antitusivo e, igualmente, no recibió aprobación.
Pearce N. «Adverse Reactions: the fenoterol story». Auckland University Press. 2007. ¿Por qué ha tardado tanto tiempo? ¡Porque no encontró ninguna revista médica que quisiese publicar el artículo debido a las amenazas de Boehringer Ingelheim!
 |
|
Durante el tiempo que trabajó para Astra-Syntex, donde era responsable de los estudios clínicos y de la aprobación de nuevos medicamentos, el autor estudió medicina.
Antiinflamatorios no esteroideos (AINE)
El medicamento más importante de esta empresa era el naproxeno un antiinflamatorio no esteroideo (AINE) sin cortisona que se empleaba para tratar dolores e inflamaciones, por ejemplo, en caso de «torceduras de muñeca».
Hay tantos AINE como arena en el mar. Uno nuevo tendría que ser notablemente mejor que las versiones anteriores y más baratas, pero la empresa no estaba interesada en realizar un estudio comparativo. Ellos ya sabían que su medicamento no era mejor, solo más caro.
El director del estudio dividió a los pacientes con torceduras de tobillo en dos grupos. A uno se le hizo reposar y al otro no. En los pacientes con movilidad la inflamación desapareció más rápidamente que en los otros. Por lo tanto, el naproxeno no tuvo ningún tipo de impacto.
Dado que los AINE cuentan con numerosos efectos secundarios para el estómago, el corazón y los riñones, seguramente se puedan sustituir por medicamentos menos peligrosos que, con mucha probabilidad, también sean más baratos.
Otros grupos farmacéuticos también emplearon métodos agresivos para convencer de que sus AINE eran los mejores del mercado:
- Pfizer afirmaba que "piroxic.." ("Felde.."), era más efectivo que la aspirina, a pesar de estar demostrado que era peligroso, sobre todo en las personas mayores, pues la excreción más lenta provocaba que se acumulase en el cuerpo y aumentaba los sangrados estomacales;
- Eli Lilly decía estar convencida de que su benoxaprofeno (enlace en inglés) (Opren, Oraflex) era capaz de prevenir el avance de los problemas en las articulaciones. Sin embargo, callaban las graves consecuencias que tenía para el hígado;
- La supuesta buena tolerancia gastrointestinal de los coxib ("Celecox..", "Etoricox..", "Rofecox..", "Lumiracox.." y "Parecox..") vino acompañada de graves efectos secundarios en el sistema cardíaco (inhibidores selectivos de la COX-2).
En su tesis doctoral «Sesgos en los estudios con doble ciego», Peter C. Gøtzsche demostró que muchos estudios se diseñan para que los resultados sean favorables a la empresa que está detrás del medicamento y contra el fármaco de control (patrocinio).
2.2. El crimen organizado como modelo de negocio de las grandes farmacéuticas
La industria farmacéutica no hace mención a las ventajas y desventajas de sus medicamentos, solo a su eficacia y seguridad. Cuando los médicos prescriben medicamentos y los pacientes los toman, ambos están convencidos de que la industria farmacéutica ha probado dicho fármaco a conciencia y de que las autoridades competentes han revisado los estudios pertinentes con mucho cuidado antes de aprobarlo (página 53).
Las compañías farmacéuticas intentan transmitir la impresión de que lo hacen, pero ni siquiera buena parte de sus empleados creen que sus jefes sean honestos.
Ejemplos de sentencias
En 2012, Pfizer pagó 60 millones de dólares para paralizar una investigación por sobornos en el extranjero (disfrazados de costes por formación, flete, etcétera).
Entre los años setenta y finales de los noventa, un «cártel» de fabricantes de vitaminas (Vitamin Inc.) dirigido por Hoffmann-La Roche se encargó de que los precios de las vitaminas se mantuviesen altos. Una vez se descubrió la conspiración, parte de los gerentes terminaron en prisión durante un pequeño periodo de tiempo y se llegaron a pagar multas de hasta 500 millones de dólares. Sin embargo, estas no supusieron más que un pequeño porcentaje de todo lo que se había ganado con la manipulación de los precios.
En el periodo de entreguerras, Roche inundó el mercado negro de Estados Unidos con opio, morfina y heroína. Y, en otros países, distintas empresas se ocuparon de estos menesteres. Encontrará más información en el libro Corporate Crime in the Pharmaceutical Industry de John Braithwaite. Editorial Routledge & Kegan Paul, Londres, 1984.
A principios de los años setenta, Roche tuvo que pagar multas por obstruir la venta de los tranquilizantes "Vali.." y "Libri.." a la competencia. No fue hasta 27 años, tras la publicación de varios estudios que advertían de que medicamentos eran adictivos, que las autoridades reconocieron este hecho.
Cita del autor:
En mi opinión y desde un punto de vista ético, es irrelevante que algunos medicamentos que influyen en el cerebro sean legales y otros no. Lo que es determinante es lo que la industria farmacéutica hace a la población. (pág. 58)
 |
|
El «salón de la verguenza» de la industria farmacéutica
Aunque el British Medical Journal (BMJ) y el New York Times publican artículos casi todas las semanas sobre el comportamiento inadecuado de las empresas, estas responden que son casos aislados.
Para determinar si eso era cierto, en 2012 el autor tomó el nombre de las diez empresas farmacéuticas más importantes, las combinó con la palabra «estafa» y las introdujo en un buscador. Estos son los resultados que obtuvo:
Pfizer, Novartis und Sanofi-Aventis
Pfizer accedió a pagar en 2009 2,3 billones de dólares cuando se descubrió que la empresa había lanzado al mercado cuatro medicamentos sin la correspondiente autorización. La empresa firmó un acuerdo de integridad empresarial de cinco años, pero seguramente le importase tan poco como los tres que había firmado anteriormente. Uno de estos medicamentos fue el antibiótico Zyvoxid (cuyo principio activo es "linezol.."), que causó varias muertes, pues la empresa afirmó falsamente que este era más efectivo en infecciones graves que la vancomicina, el medicamento convencional. De alguna manera tenían que justificar que costase ocho veces más.
Novartis tuvo que pagar en 2010 423 millones de dólares por comercializar "Trilept..", un medicamento para la epilepsia (oxcarbazepina), para usos no autorizados (dolores y psicosis), algo que hizo con cinco medicamentos más.
Sanofi-Aventis acordó pagar 95 millones de dólares en 2009 por fraude, ya que había aumentado el precio de sus medicamentos para Medicaid de forma fraudulenta.
GlaxoSmithKline, AstraZeneca und Roche
GlaxoSmithKline (GSK) pagó 3 millones de euros en el acuerdo por fraude más grande en la historia de Estados Unidos por comercializar medicamentos para usos no aprobados. Este fue el caso, por ejemplo, del antidepresivo Wellbrutin ("Bupropi..") para la pérdida de peso o de "Avand.." (rosiglitazona, enlace en inglés), un medicamento para la diabetes, debido a sus supuestos efectos positivos para el sistema circulatorio. Más tarde, el medicamento se retiró del mercado por provocar insuficiencia cardíaca.
AstraZeneca tuvo que pagar 520 millones de dólares por fraude en 2010. La empresa había recomendado su antipsicótico "Seroqu.." (neuroléptico) (quetiapina), entre otros, a niños y personas mayores para usos no aprobados como agresividad, ansiedad, demencia, alzhéimer, TDAH, es decir, trastorno por déficit de atención con hiperactividad, depresión y trastorno del sueño.
Roche ni siquiera llegó a los tribunales por el mayor robo de la historia (pág. 63). Basándose en estudios independientes, la empresa afirmó que "Tamif.." (oseltamvir) reducía de forma significativa los ingresos hospitalarios debidos a la gripe o otras complicaciones.
En 2009, Roche consiguió convencer al gobierno de Estados Unidos y a numerosos países europeos para que adquirieran grandes cantidades de "Tamif.." por miles de millones de euros y de dólares y, de esta forma, prevenir una epidemia de gripe.
GlaxoSmithKline, Johnson & Johnson, Merck, Eli Lilly und Abbott
Ni "Tamif.." ni "Relen.." ("zanamiv.."), el fármaco de GlaxoSmithKline han tenido más efecto en la gripe que un simple placebo. Un empleado de la FDA (Food and Drug Administration) quiso negarse a que aprobaran "Tamif.." y "Relen..", pero tuvo que retirarse por presiones de Roche (pág. 64). Aunque "Tamif.." no era efectivo en realidad, sí que tenía algunos efectos secundarios desagradables: alucinaciones y extraños accidntes.
Johnson & Johnson pagó en 2012 una multa de 1,1 mil millones de dólares por haber minimizado los riesgos del "Risperd.." (risperidon), un antipsicótico. J&J y su filial Janssen habían declarado que su medicamento tenía menos efectos secundarios que otros fármacos del mismo grupo, por lo que también podía administrarse a niños y personas mayores.
Merck hizo frente a una multa de 670 millones de dólares en 2007 por fraude, ya que no brindó a los programas de salud gubernamentales de Estados Unidos descuentos razonables.
Eli Lilly pagó 1,4 mil millones de dólares en 2009 por comercializar "Zypre..", un antipsicótico (olanzapina) para numerosos usos no aprobados: demencia, alzhéimer, depresiones en niños y personas mayores. Asimismo, minimizó los efectos secundarios (problemas de corazón, inflamación en los pulmones, aumento de peso considerable). Encontrará más información en el vídeo en alemán «Der DiabetesMythos» (El mito de la diabetes).
Abbott pagó 1,5 mil millones de dólares en 2012 por fraude, ya que comercializó "Depako.." (ácido valproico) para usos no autorizados.
La lista sigue
Por supuesto, podríamos seguir añadiendo casos a esta lista:
Sanofi-Aventis falsificó su estudio sobre el antibiótico "Ket.." ("Telithromyc.."), pero, a pesar de ello, la FDA se lo aprobó. Sin embargo, no hubo que esperar mucho tiempo para que se produjese la primera muerte por fallo hepático. El medicamento sigue vendiéndose, pero ahora le acompaña una advertencia en el envase y un prospecto de 26 páginas.
AstraZeneca, por ejemplo, pagó sobornos para que Medicare adquiriese un medicamento más caro. Johnson & Johnson sobornó a responsables y médicos de hospitales de distintos países para que empleasen sus productos.
Está prohibido expulsar del mercado a los fabricantes de medicamentos genéricos una vez ha expirado la patente (página 73). Glaxo inició un proceso civil para evitar la introducción de un genérico. En Estados Unidos, una empresa puede llevar a cabo este tipo de acciones y, con ello, mantener fuera del mercado un producto durante 30 meses.
Durante décadas, Bristol-Myers Squibb bloqueó la entrada al mercado de medicamentos para el cáncer más baratos (genéricos) pagando al fabricante. Lundbeck pagó grandes sumas de dinero a los fabricantes del genérico "Cipram.." ("Citalopr..") para poder continuar vendiéndolo aún más caro.
La empresa Purdue Pharma afirmó falsamente que su opioide "Oxycont.." ("Oxicodo..") era menos adictivo que otros derivados de la morfina.
En 2004-2005 el Health Committee de la British House of Commons puso a la industria farmacéutica en el punto de mira. Manifestaron que el sector compraba a médicos, políticos, instituciones benéficas, grupos de pacientes y periodistas y que sus acciones no estaban lo suficientemente reguladas.
En el informe se declaraba que limitar la influencia de la industria sería beneficioso hasta para ella misma, ya que podría volver a centrarse en desarrollar nuevos medicamentos en lugar de gastar dinero en corruptelas. El gobierno británico no hizo nada al respecto, pues, al fin y al cabo, la industria farmacéutica es el tercer sector más rentable del país.
La industria farmacéutica se puede considerar «Crimen organizado»
Como prueba de que la industria farmacéutica entra en la categoría de crimen organizado
, el autor cita una ley estadounidense, la ley RICO (Ley de Chantaje Civil, Influencia y Organizaciones corruptas), con la que se combate a la mafia y a otras organizaciones similares. La ley trata los siguientes delitos: extorsión, fraude, tráfico de drogas, sobornos, malversación, obstrucción judicial y policial, manipulación de testigos o corrupción política, entre otros. (pág. 79)
El número de acuerdos y multas por conducta incorrecta de los grupos farmacéuticos ha aumentado enormemente en los últimos años. Las empresas afirman que dichas acusaciones son viejas y que las prácticas han cambiado totalmente en los últimos años, pero eso no es verdad.
2.3. Muy pocos pacientes se benefician de los medicamentos
En este capítulo, el autor explica la importancia de los estudios de doble ciego. En este tipo de estudios, ni el paciente ni el médico saben quién ha recibido medicamento y quién placebo. La valoración de la eficacia varía según el porcentaje de los investigadores y de los sujetos que no es «ciego».
Placebos activos
El autor también explica que los pacientes a menudo reconocen si están recibiendo un placebo porque no tienen efectos secundarios.
Durante algún tiempo se emplearon placebos activos. Estos provocaban, por ejemplo, sequedad bucal, de forma similar a como sucede con algunos fármacos. Pero esto no le venía bien a la industria farmacéutica.
En muchos de estos estudios se obtenía una eficacia baja del fármaco, que se inflaba mediante operaciones matemáticas. Otras veces, el estudio se repetía hasta obtener el resultado deseado.
Una forma práctica de saber cuántas personas se benefician del tratamiento es el «Number Needed to Treat» (NNT), es decir Número necesario a tratar (enlace en inglés). Ejemplo de ello es la estatina, de la que el autor explica que no se informa del NNT porque los pacientes con colesterol alto no se benefician del tratamiento, aunque sí sufren dolores musculares y ven su calidad de vida reducida.
2.4. Estudios clínicos: un contrato social con los pacientes roto
Desde que la industria farmacéutica tiene el monopolio de los estudios que se realizan en sus productos y solo publica aquellos que le son rentables, rompe el contrato social una y otra vez.
La industria modifica los objetivos del estudio cuando no obtiene los resultados deseados o diseña otros estudios para que los resultados sean difíciles de refutar.
Nuestros gobiernos han fallado tanto en regular a las poderosas empresas farmacéuticas como en proteger la objetividad científica y la curiosidad académica de los intereses comerciales.
Resultados engañosos y maquillaje de datos
En la primera mitad del siglo XX, los medicamentos apenas se probaban antes de lanzarse al mercado, lo que provocó casos como el escándalo del Contergan (enlace en alemán) (talidomida).
El fabricante Grünenthal GmbH recomendaba su medicamento, entre otras cosas, para aliviar las náuseas matutinas durante el embarazado. Poco después empezaron a nacer niños en todo el mundo a los que les faltaban extremidades. A partir de entonces se introdujeron extensos estudios con animales para comprobar la eficacia de los medicamentos. Sin embargo, gran cantidad de medicamentos antiguos siguieron en el mercado.
Resulta problemático que para obtener la aprobación la industria farmacéutica solo necesite dos estudios de doble ciego en los que obtenga un efecto significativo a nivel estadístico.
Una empresa farmacéutica tiene numerosas formas de manipular sus estudios clínicos y de asegurarse de que los resultados benefician a sus representantes farmacéuticos, sin importarles cuáles hubieran sido los resultados de haberse llevado a cabo un estudio científico serio. Las manipulaciones son tan frecuentes y graves que uno de mis compañeros de trabajo declaraba que deberíamos contemplar los estudios más como un anuncio del medicamento que como otra cosa. A esto le respondí que los estudios de las empresas farmacéuticas ni siquiera cumplen con la regulación de la UE en materia de publicidad. (pág. 99)
En el caso de tres importantes estudios cardiovasculares realizados por investigadores independientes se observó un gran sesgo, pues cada uno de ellos obtuvo resultados favorables para el medicamento de la empresa que les estaba patrocinando. El nombre de los medicamentos, los estudios y los patrocinadores fueron los siguientes: "Prasugr..", del estudio TRITON para Daiichi Sanyko y Eli Lilly, y el estudio PLATO para Ticagrelor de AstraZeneca, en el que el número de ataques al corazón se duplicó en comparación con otros medicamentos.
Cuando el estudio principal no aporta nada positivo, siempre se pueden refugiar en los análisis de los subgrupos.
La práctica de tamizar los datos hasta encontrar por casualidad algo que se pueda aprovechar se conoce como «maquillaje de datos».
Por ejemplo, un maquillaje de este tipo fue el que condujo a la recomendación de prescribir altas dosis de cortisona a los pacientes con lesiones medulares. 14 años y miles de muertos después, se determinó que de los 31 pacientes que habían sido tratados con cortisona en lugar de con placebo, uno había muerto.
Mientras sean las empresas las que sigan decidiendo el diseño del estudio y los datos solo se puedan revelar con su consentimiento, no debería extrañarnos que los medicamentos cada vez sean más caros, pero no mejores.
Fortune 500 (Informe de 2012 sobre las empresas con más volumen de ventas): Las ganancias de las diez empresas farmacéuticas con mayor volumen de ventas superan los beneficios totales de las 490 empresas restantes.
El gigantesco estudio CRASH de la revista médica The Lancet sobre los efectos de los esteroides en 10 000 personas con lesiones cerebrales determinó que estos son muy perjudiciales. De los 31 pacientes a los que se trató con esteroides en lugar de con placebo se produjo además una muerte adicional (enlace en inglés). Miles de pacientes con lesiones cerebrales o de médula espinal murieron porque se les habían administrado esteroides y el New England Journal of Medicine y su forma de maquillar los datos son responsables de muchas de estas muertes.
Más enlaces en inglés: «Why we can't trust clinical guidelines» (Por qué no podemos confiar en las directrices clínicas). (pág. 111)
2.5. Conflictos de intereses en las revistas médicas
A las revistas médicas cada vez les resulta más complicado encontrar autores independientes de la industria farmacéutica. También les puede resultar difícil rechazar artículos «a favor de la industria», pues en tal caso pierden reimpresiones y publicidad de la propia industria.
Esto lo confirmó el antiguo editor del British Medical Journal.
New England Journal of Medicine (NEJM)
Según el autor, esto afecta de manera especial al New England Journal of Medicine (NEJM). El autor pone como ejemplo un fármaco de Pfizer para tratar las infecciones fúngicas invasivas. Se realizaron dos estudios:
En un estudio, el "Voriconaz.." ("Vfe..") fue significativamente inferior al fármaco de comparación, la anfotericina b liposomal según el plan de análisis formulado previamente y tal y como el personal de al FDA destacó en una carta posterior. Sin embargo, el artículo determinó que el Voriconazol era una alternativa viable. En el grupo del Voriconazol fallecieron más pacientes y la reducción, en teoría, muy significativa de las infecciones fúngicas invavivas se disolvió en el aire una vez se empezaron a considerar infecciones que se habían excluido del estudio de forma arbitraria. El resumen contenía resultados manipulados. (pág. 116)
Los otros estudios emplearon anfotericina b desoxicolato para comparar. Sin embargo, los efectos de este medicamento se vieron afectados al no requerir una medicación previa que redujese la toxicidad relacionada con el uso del medicamento intravenoso, aunque la duración prevista del tratamiento fueran 84 días. Los efectos tóxicos en los riñones podrían haberse reducido con una sustitución de electrolitos y agua.
Al Voriconazol, el nuevo fármaco para tratar las infecciones micóticas graves (micosis), se le dieron 77 días para actuar, mientras que al fármaco de comparación tan solo tuvo diez.
Esto invalidaba completamente la comparación. En la última frase del resumen podía leerse: 'En pacientes con aspergilosis invasiva, el tratamiento inicial con Voriconazol dio mejores resultados y una mayor tasa de supervivencia; se apreciaron menos efectos secundarios graves que en el tratamiento inicial estándar con anfotericina b'. De un estudio cuyo diseño tiene serios defectos no se puede inferir una conclusión.
Con la publicación de estudios falsos como este, el New England Journal of Medicine no solo gana bastante dinero con la venta de las reimpresiones, sino que también aumenta su factor de impacto o de influencia, que se multiplica cuando otras estudios citan la publicación. Esto sucede porque son las mismas empresas las que se sirven de distintos escritores fantasma para que publiquen estudios secundarios en los que se citen los resultados del estudio. (pág. 117)
El autor muestra el fracaso de varios estudios y pone como ejemplo otro estudio lleno de errores que el NEJM publicó y en el que se recomendaba, sin ningún sentido —según el autor—, que se administrase fluticasona (cortisona, es decir, glucocorticoides) a pacientes con pulmones de fumador. Las revistas de especialidades lo tienen especialmente difícil. Dependen de menos empresas y autores.
Según el autor, el British Medical Journal (BMJ) es una revista muy independiente.
2.6. El poder corruptor del dinero fácil
El autor narra su propia experiencia para explicar cómo empieza la corrupción. Él participó en la conferencia de un estudio llevado a cabo por una empresa en particular. Por la tarde, el jefe del departamento de ensayos clínicos le entregó un sobre lleno de dinero.
Al principio se trata de cantidades que podrían coincidir con los servicios prestados. Sin embargo, con el tiempo estas se vuelven más altas, hasta que los afectados dejan de darse cuenta de que reciben dinero de manera desproporcionada. Por supuesto, a partir de entonces tienen una obligación con la empresa de recomendar medicamentos más caros y, seguramente, también peores, o de utilizarlos en sus departamentos, aunque haya genéricos más baratos.
Amigos influyentes en la política y en la justicia

Nota de EE: Encontrará más información acerca del sobre en la página 121. «Incluía una carta en la que me agradecían mi intervención en la conferencia y un billete de 1000 dólares. No había visto en mi vida un billete tan grande y entendí que es así como la corrupción empieza».
En mi opinión, debe tratarse de un error de traducción, pues los billetes de mil dólares se imprimieron por última vez en 1945 y se retiraron en 1969. Sin embargo, siguen considerándose de curso legal.
Wikipedia al respecto: «Los billetes con un valor superior a 100 dólares ya no se emiten, aunque se consideran de curso legal, pero hoy en día su valor como objeto de coleccionismo es superior a su valor nominal. La mayor parte de los ejemplares que todavía están en circulación son propiedad de coleccionistas y de museos».
Por su puesto, las empresas farmacéuticas también tienen amigos influyentes en la política y en la justicia.
Un funcionario de la oficina del Inspector General (Tribunal de cuentas) de Pensilvania señaló que Pfizer y Jansen habrían transferido dinero negro a cuentas de funcionarios de la institución para que trabajaran en una serie de directrices que recomendaran la sustitución de medicamentos viejos y más baratos por nuevos y, por supuesto, más caros. Por estas declaraciones, su supervisor le indicó que no volvería a trabajar allí, ya que la industria farmacéutica pagaba a ambos bandos.

Nota de la doctora en medicina LÖ: la afirmación que toma de «The Drug Pushers», de The Atlantic, en la que se dice que una pizza o un bolígrafo hacen tanto por la confianza en sí mismos de los médicos que abre la puerta a que se les puede sobornar en un futuro me parece un insulto para los «médicos de a pie» de la base de la pirámide, que son los que verdaderamente trabajan con los pacientes. Ni nuestra autoestima es tan baja ni valemos tan poco como para prescribir algo en lo que no creemos.

EE: La afirmación: «Un regalo en particular no influye, pero sí que puede hacer a un doctor darse cuenta de que no aceptaría regalos más grandes en un futuro. Una pizza o una linterna de bolsillo son como inoculaciones, pequeñas inyecciones de autoestima que hacen creer al doctor que el dinero nunca le corromperá».
2.7. ¿Qué hacen miles de médicos con el dinero que reciben de la industria?
Una pequeña parte de los médicos trabaja en realidad en investigación. La mayoría ayudan a las empresas a que vendan sus productos. Esto es necesario porque cada vez es más raro que haya medicamentos verdaderamente nuevos y buenos.
Seeding Trials (estudios sin valor científico ni grupos de control)
Para vender los 106 productos innecesarios hacen falta muchos ayudantes. Así pues, las empresas patrocinan estudios clínicos que en realidad solo sirven para dar argumentos a los departamentos de marketing.
De este tipo de estudios, los peores son los seeding trials (enlace en inglés). Estos son estudios sin ningún tipo de valor científico ni grupos de control. A los médicos se les da un arsenal del nuevo medicamento y se les paga por cada paciente al que prescriben el fármaco. En general, los médicos creen que en realidad están haciendo algo por la ciencia.
Los líderes de opinión salen caros. Reciben mucho dinero por prestar su nombre para hacer una recomendación o no escribir un artículo negativo sobre un medicamento malo o demasiado caro.
Terapias de sustitución hormonal (TSH)
Las empresas también necesitan un buen número de conferenciantes en las reuniones que ellos mismos patrocinan para que expliquen por qué el producto de la empresa es mejor y si se puede emplear o no para indicaciones no aprobadas.
Un ejemplo infame de indicaciones sin aprobación fue lo que sucedió con las terapias de sustitución hormonal (TSH) para las mujeres hasta el final de sus vidas. Se alabó a los cuatro vientos su capacidad para prevenir enfermedades coronarias, hasta que se descubrió que en realidad favorecían su aparición.
Véase el Million Women Study.
 |
|
2.8. Estrategias de ventas agresivas
Los estudios clínicos de las empresas suele ser marketing encubierto. El autor lo ilustra con un estudio sobre un antirreumático con muy pocos sujetos de prueba.
Otro ejemplo serían los estudios de medicamentos para el colesterol (estatina), en los que el fármaco de la empresa conseguía mejores resultados que el producto de la competencia.
Si A es mayor que B y B es mayor que C, entonces C no puede ser mayor que A
Gøtzsche nos muestra numerosos trucos y ejemplos y explica uno de ellos de forma más detallada:
Por qué la olanzapina es mejor que la risperidona, la risperidona mejor que la quetiapina y la quetiopina mejor que la olanzapina: un análisis exploratorio de los estudios comparativos sobre antipsicóticos de segunda generación. Desde un punto de vista matemático, esto no puede ser cierto. Si A es mayor que B y B es mayor que C, entonces C no puede ser mayor que A.
Como ya se ha mencionado anteriormente, se permite que haya artículos escritos por escritores fantasma. Estos se citan en otros artículos y en material promocional como si fuesen de otro autor. Lo mejor es conseguir que quien lo haga sea un renombrado experto, que presta su nombre pero no tiene ninguna influencia en el contenido del artículo. Cuando un autor potencial exige cambios, el artículo se publica con el nombre de otro investigador. (pág. 151)
El profesor y doctor en medicina David Healy explicó (enlaces en inglés) lo habitual que es que algunas empresas se posicionen en contra de los médicos. Por ejemplo, él recibió el siguiente escrito: Nuestro escritor fantasma nos ha enviado un primer borrador basado en su trabajo publicado. Se lo adjunto.
Como el profesor Healy (enlace en inglés) estaba descontento con la excesiva alabanza al medicamento y propuso cambios, recibió más tarde una respuesta en la que se le informaba de que había perdido algunos puntos de importancia comercial y la empresa publicó el artículo con el nombre de otro investigador.
Sin embargo, para que la comercialización sea un éxito no hacen falta fuentes. Una campaña publicitaria agresiva también es efectiva, como explica el autor que sucedió con el inhibidor de ácido gástrico Zantac (ranitidina).
Doch für ein erfolgreiches Marketing braucht man nicht unbedingt Literatur. Eine aggressive Werbekampagne tut es auch, wie der Autor am Beispiel des Magensäurehemmers Zantac (Ranitidin) beweist.
Inhibidor de ácido gástrico Zantac (ranitidina)
Hasta 1977, las úlceras estomacales solían operarse y, en ocasiones, los pacientes morían por sangrado de estómago. Entonces, James Whyte Black, de la empresa Smith Kline & French, desarrolló la cimetidina, que salió al mercado en el año 1976 como Tagamet. Esto le llevó a recibir el premio Nobel en el año 1988.
En 1983, GlaxoSmithKline comercializó un fármaco muy similar: la ranitidina como Zantac. No era mejor, pero que costase un 50 % más así lo sugería. Además, esto vino acompañado de una campaña publicitaria brutal que convirtió la acidez estomacal en la enfermedad generalizada más tratada.
Tres años después, el Zantac era el fármaco más vendido en todo el mundo. En la página de Wikipedia en alemán podemos leer: La ranitidina es unas diez veces más potente que la cimetidina, pero tiene muchos menos efectos secundarios.
Hoy en día se comercializan genéricos de ranitidina como Junizac (D), Pylorisin (A), Ranic (A), Ranicux (D), Ranimed (CH), Raniprotect (D), Ranitic (D), Sostril (D), Ulcidin (CH), Ulsal (A), Zantac (A), Zantic (D, CH), entre muchos otros.
Para las empresas es mucho más lucrativo gastar dinero en publicidad, muestras de medicamentos, formación patrocinada, expertos a sueldo y representantes farmacéuticos que hacer investigaciones y estudios serios.
Viajes promocionales al Caribe
En cualquier caso, invitar a los expertos adecuados a un viaje promocional por el Caribe merece la pena. Por poner un ejemplo, el autor explica cómo después de unas vacaciones pagadas tras la introducción de un nuevo antibiótico y de un fármaco para el corazón, estos se empleaban tres veces más en las clínicas.
Ejemplo de ello es el Ondansetrón, un fármaco que alivia las náuseas provocadas por la quimioterapia. El autor expone cómo la firma se empeñó en probar su eficacia también en las náuseas del postoperatorio. Cuando la patente expiró, parece que también lo hizo el efecto.
Libros sobre las interacciones menos deseadas entre las empresas farmacéuticas y los médicos
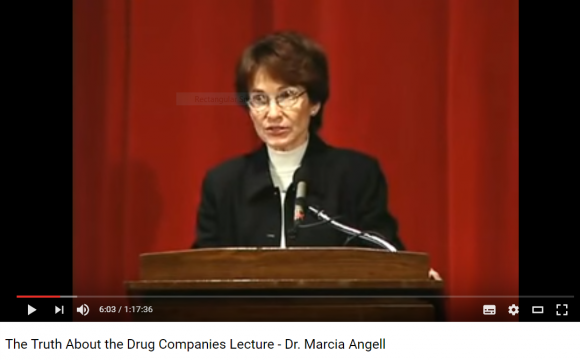
Antiguos editores del NEJM y del BJM han escrito distintos libros sobre las interacciones menos deseadas entre la industria farmacéutica y los médicos: «The Truth About the Drug Companies, how they deceive us and what to do about it» de la doctora en medicina Marcia Angell (enlace en inglés) (n. 1939), New York, 2004, Random House.
El libro de la doctora en medicina Marcia Angell también se encuentra disponible en español bajo el nombre «La verdad acerca de la industria farmacéutica: cómo nos engaña y qué hacer al respecto».
El libro «On The Take: how medicine's complicity with big business can endanger your health» del profesor y doctor en medicina Jerome P. Kassirer, Oxford University Press, 2005, incluye las siguientes declaraciones:
A algunos médicos se les conoce como putitas.
El término empleado no deja lugar a dudas. Kassirer era un profesor de Medicina con gran experiencia y se expresaba con total claridad. Como Kassirer era honesto, perdió su puesto como editor jefe, pero su sucesora, Marcia Angell también fue recta y honesta.
El libro «The Trouble with Medical Journals» de Richard Smith, 2006, Taylor & Francis Ltd refleja el problema de las publicaciones médicas.
En la revista de la Royal Society of Medicine (JRSM, enlace al texto en inglés) también se puede encontrar un artículo importante al respecto. En el artículo, la JRSM apunta: «Richard Smith fue editor del BMJ y director ejecutivo de BMJ Publishing Group durante 13 años».
 |
|
Poniendo como ejemplo los biomedicamentos (biofármacos) en casos de artritis reumatoide, Peter C. Gøtzsche muestra cómo los expertos emiten recomendaciones para medicamentos muy caros, aunque una combinación de dos medicamentos básicos y baratos podría lograr el mismo efecto.
También describe ejemplos sobre caros medicamentos para tratar el cáncer que, por ejemplo, solo prolongan la supervivencia en diez días, pero disminuyen la calidad de vida. A menudo, un tratamiento barato para el dolor sería más adecuado para los pacientes.
Pfizer, Doxazosina y el estudio ALLHAT
En el estudio ALLHAT (enlace en alemán) se compararon diferentes fármacos para tratar la hipertensión y se determinó que la doxazosina de la empresa Pfizer era menos efectiva que otros medicamentos. Por este motivo, el American College of Cardiology (Colegio estadounidense de cardiología) recomendó suspender la doxazosina, pero cambió de idea unas horas después, tras las quejas de Pfizer. Después de todo, la empresa dona medio millón de dólares al colegio.

Wikipedia refleja este estudio como otros también lo han hecho: cuando de un estudio a gran escala y doble ciego se obtienen resultados perjudiciales, la industria contraataca —al igual que sucede en la industria láctea— con numerosos estudios que afirman lo contrario y a los consumidores solo les queda la siguiente frase: «Los resultados del estudio siguen siendo controvertidos».
Después de todo, ¿quién se atrevería a poner en entredicho a grandes empresas consolidadas? A menudo, sus ayudantes también están dentro de Wikipedia y bloquean cualquier corrección.
Como ejemplo de expertos a sueldo de la industria farmacéutica, Peter C. Gøtzsche habla del presidente de la Sociedad danesa para la Hipertensión, que siempre recomienda los medicamentos más novedosos y caros de las empresas que le patrocinan.
Un ignominioso papel juegan también, por ejemplo, los grupos de apoyo organizados por la industria. Y sus miembros no suelen ser conscientes de que las empresas les utilizan para introducir medicamentos caros y, a menudo, ineficaces.
2.9. Supervisión de los medicamentos inadecuada
Por supuesto, hay organismos estatales que se encargan de aprobar los medicamentos, pero dado que son las mismas empresas las que realizan los estudios, los encargan o al menos los supervisan y solo tienen que presentar los informes después, emplean varios trucos para encubrir los efectos adversos. Por ejemplo, una manera de ocultarlos es llenar múltiples estanterías de informes y esconder una página con los efectos secundarios peligrosos entre todas las hojas.
Las autoridades encargadas de supervisar los medicamentos tienen conflictos de intereses. Podría decirse que algunos funcionarios trabajan casi a media jornada para las empresas a las que deberían supervisar o, incluso, se preocupan por sus acciones. Y, cuando tienen que dejar su puesto oficial tras un gran escándalo, les esperan puestos aún más lucrativos en la industria farmacéutica.
Ejemplos
El empleado que aprobó "Vio.." se convirtió en un importante consultor para Merck, la empresa fabricante de "Vio..". "Vio.." es un antirreumático que tuvo que retirarse posteriormente del mercado por sus graves efectos secundarios para el sistema cardiovascular.
Cuando se producen efectos secundarios graves e inesperados, suele llevar un tiempo retirar el medicamento del mercado, por un lado, porque no se quiere perjudicar a la empresa y, por el otro, porque las autoridades no quieren quedar en evidencia por haber aprobado un fármaco de forma negligente. El bienestar de los pacientes pasa a un segundo plano.
Antiguos trabajadores de la Food and Drug Administration (FDA) estadounidense, la agencia responsable de la regulación de los medicamentos, informaron de corrupción generalizada e intimidación y traslado de funcionarios a los que no se había podido sobornar. Se les vigilan los ordenadores y, a veces, incluso se amenaza sus seres queridos. (pág. 179)
Cuando se publicó un nuevo reglamento sobre prospectos, la agencia añadió un nuevo párrafo sin avisar una vez hubo expirado el plazo de objeción. Dicho párrafo excluye procesos judiciales por responsabilidad del producto, aunque la empresa no haya advertido de un determinado riesgo, a menos que el paciente pueda demostrar que la empresa le ha engañado de forma deliberada. (pág. 178)
En 1993 estalló un escándalo de sobornos en Italia en el que se vieron involucrados el ministro de salud, el jefe del departamento responsable de la adquisición de fármacos en el Ministerio y varios investigadores. Todos ellos desempeñaron diferentes papeles en la aprobación de medicamentos encarecidos y, a veces, peligrosos, y provocaron pérdidas al estado de tres mil millones de dólares.
La insoportable levedad de los políticos (pág. 183)
En Estados Unidos, la industria farmacéutica dona generosamente a campañas electorales y eventos políticos. Cada congresista tiene detrás a más de un grupo de presión. Los republicanos tienen a la mayoría. ¡Por ello, en 1994 intentaron suprimir la FDA y dejar la aprobación y el seguimiento de los medicamentos en manos de la industria farmacéutica!
Ventajas para la industria
En 2002 se revocó el nombramiento de un nuevo comisario de la FDA porque puso demasiado énfasis en la seguridad de los medicamentos.
La industria se ha beneficiado de los plazos cortos en los que los medicamentos reciben la aprobación sin pruebas suficientes. Dichos plazos acelerados estaban previstos, en un principio, para la aprobación urgente de medicamentos vitales. Es más que cuestionable que este sea el caso con determinados medicamentos para la diabetes de tipo 2, dolores u obesidad —ha habido que retirar medicamentos de los tres tipos debido a efectos secundarios graves.
El buen trabajo de los grupos de presión llevó a la Comisión Europea la absurda propuesta de comercializar los fármacos aunque no fueran lo suficientemente efectivos.
La organización de consumidores Health Action Europe (HAI) protesta por estas y otras prácticas peligrosas. Lo lógico sería que de eso se encargasen los políticos. (pág. 188)
Solo ha habido pequeños avances: La Agencia Europea del Medicamento (European Medicines Agency, EMA), la FDA europea, por así decirlo, ya no se encuentra dentro de la dirección general de Empresa e Industria, sino en Sanidad y Consumo. Además, se ha relajado el estricto reglamento de privacidad en la regulación de medicamentos.
La teoría económica predice que las empresas modificarán sus principios cuando las ganancias superen los costes. Si la detección es costosa para las administraciones, podemos esperar modificaciones en esos principios
, según el profesor y doctor Alan Maynard, un conocido economista de la salud británico. (pág. 191)
GlaxoSmithKline, el estudio SMART y los tratamientos para el asma
La industria manifiesta una y otra vez que la regulación de los medicamentos se basa en la confianza. Pero, ¿por qué debemos creernos que un medicamento no provoca cáncer únicamente porque las ratas que se han empleado en los estudios no lo han padecido, ya que han muerto mucho antes por los efectos secundarios? (EE: Nosotros vivimos mucho más que las ratas, que viven unos dos o tres años).
El autor expone el estudio Smart de GlaxoSmithKline sobre los casos de muerte por "salmeter.." (la crítica solo aparece en el artículo de Wikipedia en inglés) un beta antagonista de acción prolongada para personas asmáticas. GlaxoSmithKline envío a la FDA datos manipulados. El estudio duró 28 semanas, pero si los investigadores hubieran querido, podrían haber informado de los efectos secundarios que se produjeron durante los seis meses posteriores.
La empresa incluyó en el estudio los datos del periodo de seguimiento y admitió, únicamente cuando se le preguntó por ello, que solo parte de ellos procedían de un estudio aleatorizado doble ciego. El estudio descubrió un aumento del número de muertes en los pacientes con asma a los que se había tratado con "salmeter..". El autor recomienda retirar el "salmeter.." del mercado, mientras que la FDA se limita a aconsejar su uso cuando el resto de medicamentos fallen.

La doctora en medicina LÖ: ¿Qué otros medicamentos? Como médica veterana he convivido con los siguientes medicamentos: altas dosis de cortisona, atropina, adrenalina (en estado asmático es devastadora para el corazón), teofinlina, antihistamínicos, parasimpáticos como anticolinérgico, también llamados parasimpaticolíticos, antagonistas de los receptores muscarínicos, antiparasimpaticomiméticos o antimuscarínicos (el ipratropio suena bien, pero en general solo es efectivo si se combina con fármacos betamiméticos), o el "Monteluka..", que es muy caro y rara vez alivia al paciente.
Desde la introducción de los beta 2 miméticos de acción prolongada, apenas tenemos ataques graves, que no son beneficiosos para el corazón, y las hospitalizaciones de nuestros pacientes asmáticos se han reducido enormemente.
Y, por raro que pueda parecer, también se están haciendo más mayores. Aquí parece haber una diferencia sustancial entre Europa y Estados Unidos. En lo que respecta a los beta miméticos de acción corta, comparto la opinión con el autor, matan a los asmáticos.
Dos estudios controlados con placebo mostraron además que no son lo suficientemente efectivos. Sin embargo, la empresa puede repetir los estudios tantas veces como desee hasta conseguir dos estudios que demuestren el efecto. Para que un medicamento se apruebe, no puede ser peor que los que ya se encuentran en el mercado. Pero, ¿cómo se puede comprobar eso si solo se prueban con placebos?
La Declaración de Helsinki y los estudios en seres humanos
En el mercado podemos encontrar multitud de medicamentos para la tos ineficaces y que se venden sin receta. Sin embargo, lo que sí tienen son efectos secundarios (alucinaciones, arritmias, etc.) y aún sí se siguen comercializando.
La Declaración de Helsinki exigía que los resultados de los estudios en seres humanos se publicasen y que la investigación médica con sujetos humanos se basase en literatura científica bien documentada. (pág. 221)
En 2008, la FDA determinó que los productos cuyos estudios se habían realizado en el extranjero podrían aprobarse en Estados Unidos, aunque estos no siguiesen las directrices de la Declaración de Helsinki. Será que jamás oyeron hablar de los juicios de Núremberg. Estados Unidos tuvo sus propios experimentos en prisioneros o el escándalo de Tuskegee, también conocido como el experimento Tuskegee, en el que durante 40 años no se trató a 399 hombres de raza negra infectados con sífilis para estudiar la evolución natural de la enfermedad.
Las personas de los países desfavorecidos son populares conejillos de indias, pues no existe el peligro de que demanden a la empresa por problemas de salud.
El ejemplo más conocido son los estudios de anticonceptivos orales realizados en Puerto Rico, Haití y México y, en fases posteriores, entre las mujeres más pobres de Estados Unidos. La corte de apelaciones estadounidense recobró esa decisión y obligó a Pfizer a acatar la Declaración de Helsinki.
Pfizer tuvo que indemnizar a las familias nigerianas cuyos hijos habían fallecido de meningitis o habían sufrido grandes daños. A los niños, sin el conocimiento de sus padres, se les había administrado un fármaco de Pfizer como parte de un estudio, aunque existía un medicamento mucho mejor. (pág. 200)
No basta un solo efecto en el resultado sustitutivo. Estos son, por ejemplo, valores de laboratorio como el nivel de colesterol, cuya reducción no tiene mayor importancia en cuanto a supervivencia o menos complicaciones de la enfermedad.
- Otro ejemplo de ello es la rosiglitazona, un medicamento que, a pesar de reducir los niveles de colesterol, aumentó el número de muertes por problemas cardiovasculares.
- Asimismo, también podríamos hablar de los fármacos para tratar las trastornos del ritmo cardíaco. Es verdad que normalizaron los electrocardiogramas, pero debido a ellos fallecieron alrededor de 50 000 personas al año.
- Por último, también pone por ejemplo los medicamentos para el cáncer que, aunque reducían el tamaño del tumor, no aumentaban la esperanza de vida.
Medicamentos con posibles efectos adversos que se aprueban aunque no haya datos suficientes sobre su seguridad
Las autoridades no deberían aprobar medicamentos con posibles efectos adversos si no hay datos suficientes sobre su seguridad. Sin embargo, se aprobaron inhibidores de la COX-2 como "Vio.." y compañía aunque su acción apuntaba a un mayor riesgo de muerte por complicaciones cardiovasculares.
Es habitual que los estudios de seguimiento a largo plazo no se realicen, ya que las multas son muy bajas. ¿Qué son 10 millones de dólares para una empresa farmacéutica? Además, cuando la lista de advertencias es infinitamente larga, casi nadie se acuerda o llega a leérsela del todo.
Un ejemplo de ello sería el prospecto de las estatinas (reductor del colesterol en sangre) según el autor, pues, aunque el fármaco redujese el nivel de colesterol en sangre, no afectaba al riesgo de padecer complicaciones cardiovasculares o incluso de morir y además podía provocar rabdomiólisis, insuficiencia renal, daños en el hígado y aumento del nivel de azúcar en sangre.
Es habitual que se aprueben medicamentos peligrosos de los que ni siquiera se sabe si son eficaces.
- Por ejemplo, cisrapid, que se comercializa como Alimix y Propulsin. Este fármaco, que en teoría favorece el vaciamiento gástrico, provocó muertes por arritmias cardíacas. Por supuesto, esto estaba reflejado en alguna parte del prospecto. Cuando el medicamento se retiró del mercado, los representantes de la empresa explicaron que ni siquiera se había comprobado que el medicamento funcionase.
Polifarmacia (multipharmacy en inglés o Polypragmasie en alemán): muchas personas, sobre todo ancianos, toman más de un medicamento al mismo tiempo. A menudo no sabemos cómo unos interfieren en los efectos del otro y, en general, cómo afectan al paciente.
Peter C. Gøtzsche interrumpe tratamientos cuando los pacientes llegan al hospital.

La doctora en medicina LÖ: a los pacientes se les retira la medicación cuando salen del hospital, por ejemplo, en el caso de medicamentos para reducir el nivel de colesterol en sangre en personas de 80 años, fármacos para tratar la tensión arterial y que se sientan «más jóvenes» (que a la vez provocan mareos) pastillas para dormir, etcétera. Pero cuando vuelven a ingresar en el hospital o ven a un especialista en medicina interna se los vuelven a prescribir.
2.10. Acceso público a los datos de las autoridades competentes
La industria farmacéutica afirma que sus estudios y los datos relativos a estos son secretos comerciales. La FDA, por su parte, explica que no puede rectificar afirmaciones incorrectas de las compañías farmacéuticas. En general, la mitad de los estudios no se publican jamás, pero aquellos que obtienen resultados favorables se publican en varias ocasiones como si fueran distintos.
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés): acceso a los datos de los estudios clínicos y transparencia
En realidad, todos los estudios (también los negativos) realizados en pacientes o con voluntarios sanos deberían estar disponibles para el público y cualquier persona interesada debería tener acceso.
En 2007, Gøtzsche y Jørgensen pidieron a la Agencia Europea del Medicamento (EMA) acceso a todos los datos relativos a los fármacos contra la obesidad. Sin embargo, este acceso se les negó debido a los intereses comerciales de las empresas. Entonces decidieron acudir al defensor del pueblo europeo, Nikoforos Diamandouros. Este determinó que los documentos no contenían ningún secreto comercial y que su publicación era de interés público.
Como, tres años después, la EMA todavía no había preparado nada para que se llevase a cabo el examen de los datos, acudieron a la prensa. En aquel momento, la EMA decidió dar la impresión de que ella siempre había estado a favor. En 2010, la EMA decidió ampliar el acceso público a los documentos, incluidos los informes finales de los estudios y los planes de ensayos. El director de la EMA dejó la agencia y fundó una empresa consultora para la industria farmacéutica.
El nuevo director, Guido Rasi, anunció que a partir de entonces el tema no iba a consistir en si los datos se iban a hacer públicos o no, sino en la forma.
Véase Agencia Europea del Medicamento: «Access to clinical-trial data and transparency» (Acceso a los datos de los estudios clínicos y transparencia). Informe del taller de 2012.
El acceso a los datos de otras agencias reguladores también es complicado. Gran Bretaña destruye los documentos a los 15 años. La FDA solo acepta solicitudes específicas, lo cual es complicado. Y también se ha sabido de casos en los que «se les han perdido páginas».
Pastillas para adelgazar
El autor expone la historia de las pastillas para adelgazar (anorexígenos) para demostrar cómo las empresas luchan a toda costa para sacar y mantener en el mercado estos medicamentos, tan peligrosos como ineficaces, a pesar de los numerosos casos mortales.
La mayoría tienen efectos similares a las anfetaminas (Upper, enlace en alemán). La pérdida de peso es de alrededor del 3 %, en comparación con el placebo, que apenas alcanza el 1,5 %. Sin embargo, pueden provocar hipertensión pulmonar, que es mortal
Otro efecto secundario es la valvulopatía, que ya se observó en estudios con ratas, pero que no impidió que la empresa Wyeth comercializase Redux. Para ello, sobornaron a empleados de las autoridades reguladoras y compraron a expertos. Lo de siempre.
2.11. "Neuront..": medicamento antiepiléptico y antitodo
En el año 2004, la empresa Pfizer pagó una multa de 27 millones de dólares por comercializar "Neuront..", un medicamento antiepiléptico cuya sustancia activa es la gabapentina, para fines no autorizados. Una nimiedad si lo comparamos con los 2700 millones de dólares de beneficios.
Representantes farmacéuticos que hablan con los pacientes en las consultas médicas
Warner-Lambert, propietario de la patente de la gabapentina, de la que más tarde Pfizer se hizo cargo, pagó a médicos para que permitiesen que sus representantes farmacéuticos recomendasen a sus pacientes y en su presencia "Neuront.." para numerosas enfermedades como, por ejemplo,
trastornos bipolares (depresión maníaca), dolores, migrañas, déficit de atención, síndrome de piernas inquietas o para desengancharse del alcohol o las drogas. Los representantes farmacéuticos que hablan con los pacientes en las consultas parecen ser bastante habituales en Estados Unidos.

La doctora en medicina LÖ: en mi trabajo nunca he vivido lo que el doctor GØTZSCHE describe, es decir, que haya personas importantes como, por ejemplo, los responsables de los departamentos de las universidades, programas clínicos o departamentos en sí a los que se ha invitado a viajes de lujo o que han recibido honorarios por dar conferencias sobre "Neuront..". A otros se les pagó para poder poner firmar con sus nombres artículos que algún escritor fantasma había redactado.
Apertura de Pfizer: Sobre la comercialización ilegal, la empresa tiene una estrategia de publicación: los resultados se publican... siempre y cuando sean favorables.
(pág. 237)
Pero, a pesar de la identificación parcial (y del estudio ciego), en la planificación del estudio para otros usos del "Neuront.." no se estableció que fuera muy efectivo, pero sí se encontraron efectos secundarios.
Pfizer nunca informó ni a doctores ni a pacientes de que el "Neuront.." no había demostrado ser mucho más efectivo que el placebo. (pág. 240)
2.12. Merck, donde los pacientes mueren primero
Incluso antes de su lanzamiento al mercado, la empresa Merck ya sabía que "Vio..", al igual que el resto de inhibidores de la COX-2b, suponía riesgo de trombosis y, por lo tanto, aumentaba también las probabilidades de padecer un ataque al corazón, ya que en los estudios clínicos había reducido la excreción de metabolitos de prostaciclina en voluntarios sanos a la mitad. Merck ocultó este efecto secundario en la siguiente frase sin sentido: los inhibidores de la COX-2 pueden desempeñar un papel en la biosíntesis sistémica de la prostaciclina.
"Vio.." provocó unas 120 000 muertes antes de que lo retirasen del mercado
No se permitió que personas con riesgo de padecer problemas cardiovasculares participasen en el estudio VIGOR. Este fue un estudio comparativo que se realizó con antiguos AINE (antiinflamatorio no esteroideo). Aunque se observaron más ataques al corazón en este estudio, que no incluía a pacientes de alto riesgo, esta información decidió omitirse.
Los estudios en los que se informaba de un mayor riesgo de padecer problemas cardiovasculares no se publicaron hasta que el medicamento se hubo retirado del mercado. El estudio VIGOR, lleno de errores, se publicó en el NEJM. Aunque diferentes científicos señalaron dichos errores, el NEJM no hizo ninguna rectificación.
Además, pese a que el riesgo de trombosis continúa incluso un año después de interrumpir el tratamiento con "Vio..", la empresa ignoró todos los resultados recogidos a partir de las dos semanas desde el fin del mismo. Según estima el autor, "Vio.." provocó unas 120 000 muertes antes de que lo retirasen del mercado.

EE: ver también "Rofecox..". Del artículo de Wikipedia en alemán: «En 2009 se hizo público que Merck había confeccionado una lista interna de críticos del medicamento a los que había que silenciar antes de retirar el mismo del mercado».
2.13. El fraudulento estudio del "Celecox.." y otras mentiras
Aquí nos encontramos con una historia similar, en este caso con "celecox.." (nombre del producto, "Celebr.."), el inhibidor de la COX-2 de Pfizer. En este caso, la empresa llevó a cabo dos ensayos: uno, frente al diclofenaco y otro, frente al ibuprofeno. Ambos contaban con distintos planes de estudio, pero los resultados favorables se resumieron y se hicieron constar como si solo se hubiese realizado un ensayo.
La empresa solo publicó datos sobre la supuesta mejor tolerancia gástrica, pero no dijo nada sobre los efectos secundarios en el sistema cardiovascular y a los pacientes afectados de este tipo de enfermedades se les retiró del estudio directamente. Cuando el aumento de muertes por ataque al corazón les fue imposible de ocultar (unos 100 000, aproximadamente) la FDA les exigió que incluyesen una advertencia en el prospecto.
"Celebr.."
Decía algo así: Los inhibidores selectivos de la COX-2 pueden estar relacionados con eventos tromboembólicos (pág. 255).
Cuando en 2004 se retiró "Vio.." del mercado, Pfizer aprovechó la ocasión para destacar que habían analizado los datos de 400 000 pacientes y que no se había advertido ningún aumento del riesgo de ataque cardiaco con "celecox..".

La doctora en medicina LÖ: hoy en día el medicamento todavía se comercializa, pero, afortunadamente, muchos sistemas de salud nacionales ya no lo subvencionan. Así que cada vez son menos los pacientes que lo adquieren. Sin publicidad descarada y agresiva, "Vio.." ni "Celebr.." jamás se hubiesen llegado a prescribir. Pero la promesa de un AINE sin efectos secundarios gastrointestinales era muy tentadora.
2.14. Medicamentos costosos para sustituir los baratos prescritos a los pacientes
Como primer ejemplo, el autor expone el cambio de personas diabéticas a insulinas nuevas y más caras. Un cambio que, en general, solo tendría sentido en casos de hipoglucemias graves y frecuentes.
Cómo las empresas siguen lucrándose de un medicamento caro cuando la patente ha expirado
Un truco que emplean las empresas cuando la patente ha expirado y quieren seguir vendiendo su medicamento más caro es el de la estereoisometría, que en inglés se conoce como «evergreening» (perenne).
Hay medicamentos que tienen dos mitades que se comportan como si fueran un espejo y en las que solo una está activa. Cuando la patente ha expirado, la empresa patenta la mitad activa e inicia una campaña publicitaria en la que destaca que el fármaco es más eficaz, lo que no es cierto, pero sí que lleva a muchos médicos a no recetar genéricos más baratos.
Esto pasó con los medicamentos para las úlceras estomacales: cuando la patente del inhibidor de la bomba de protones omeprazol (Losec, Prilosec) caducó, AstraZeneca sacó al mercado la mitad activa como esomeprazol (Nexium).
Esto, con estudios plagados de errores: por ejemplo, se emplearon 40 miligramos de Nexium frente a 20 miligramos de Losec para demostrar que una sustancia era mejor que otra (pág. 265). ¡La proporción tendría que haber sido la contraria! Pero Nexium era 30 veces más caro.

La doctora en medicina LÖ: esto me tranquiliza. Nexium nunca me impresionó y solo se lo he recetado a pacientes a los que se lo había prescrito un especialista e insistían en seguir tomando ese mismo.
La empresa AstraZeneca se gastó durante el primer año y solo en Estados Unidos 500 millones de dólares en publicidad.
2.15. Todo perfecto con los niveles de azúcar en sangre, pero el paciente muere
En este caso se trata de la rosiglitazona ("Avand.."), un antidiabético de la marca GlaxoSmithKline. Aunque los estudios comparativos de la empresa antes de su aprobación ya demostraban un riesgo elevado de ataques al corazón frente a la pioglitazona, la empresa decidió no realizar más estudios comparativos y mantuvo estos datos en secreto.
Pese a que el fármaco provocó más ataques cardíacos que los placebos o que otras sustancias activas
, la FDA aprobó el medicamento en 1999. Según el prospecto, el fármaco aumentaba el colesterol LDL en un 19 %, lo que explicaba sus efectos dañinos en el corazón. (pág. 269)
«Medicamentos milagrosos»
Un año más tarde, la EMA europea también cedió a las presiones de respetados miembros de DiabetesCommunity y aprobó el medicamento. La DiabetesCommunity no quería perderse el nuevo «medicamento milagroso».
En 2004, la OMS alertó a la empresa de los problemas del corazón e incluso informó a la FDA y a la EMA. En 2006, un estudio realizado por GlaxoSmithKline lo confirmó. Ninguna organización emitió advertencia alguna, ya que se trataba de un secreto comercial de la empresa.
Algunos científicos independientes enviaron su metaanálisis sobre la rosiglitazona al New England Journal of Medicine. Este envió el artículo a la empresa, que enseguida publicó un informe provisional sobre un estudio sin enmascaramiento (sin ciego). Tras un examen objetivo sobre los casos individuales de los pacientes en el estudio RECORD, se concluyó que la rosiglitazona suponía un mayor riesgo cardiovascular que la pioglitazona.
No es algo que nos sorprenda, pues "Avand.." aumentaba los niveles de colesterol en sangre. En 2009, la empresa inició un nuevo estudio que debería concluir en 2015. Por suerte, en Europa este fármaco se retiró del mercado. En Estados Unidos se puede seguir adquiriendo, aunque con un nuevo prospecto.
La glitazona, es decir, una tiazolidinediona, también tiene efectos poco deseables como, por ejemplo, un aumento en la incidencia del cáncer de vejiga (pioglitazona) o insuficiencia hepática, como la roglitazona (enlace en inglés), lo que llevó a que se retirase del mercado.
Otro antidiabético es la liraglutida ("Liragluti..", en inglés, "Victo..") un péptido similar al glucagón 1 (hormonas peptídicas) de la empresa Novo Nordisk. Algunos investigadores independientes concluyeron un mayor riesgo de inflamación pancreática (pancreatitis) y de cáncer (cáncer de páncreas) con "Victo.." y publicaron los resultados en la página web de la revista Gastroenterology. La empresa Novo Nordisk les exigió que retirasen el artículo.
Desde el momento de su aprobación ya se plantearon problemas de seguridad graves, pero prevalecieron los intereses comerciales.

La doctora en medicina LÖ: una curiosidad es que la única paciente nuestra a la que se le prescribió "Victo.." para controlar su diabetes padeció un cáncer de páncreas. Y el medicamento ni siquiera le ayudó en los parámetros empleados (valores de medición) de peso y nivel de azúcar en sangre.
El único medicamento que aumenta la esperanza de vida de las personas que padecen diabetes de tipo 2 es la antigua y barata metformina. El único inconveniente: en caso de daños renales, una complicación de la diabetes, no se puede prescribir.
2.16. La psiquiatría, el paraíso de la industria farmacéutica
Definir los trastornos psiquiátricos es difícil. En Estados Unidos podemos encontrar el famoso «Manual diagnóstico y estadístico de los trastornos mentales» (DSM, por sus siglas en inglés), de la Asociación Estadounidense de Psiquiatría (APA, por sus siglas en inglés). En cada nueva versión aparecen pequeños trastornos convertidos en nuevas enfermedades. Esto es peligroso, ya que las enfermedades requieren tratamiento. El DMS no se basa en resultados científicos, sino que se trata de un documento consensuado sobre el que se vota.
El autor cita a la doctora en medicina Marcia Angell, antigua editora del New England Journal of Medicine: He pasado gran parte de mi vida evaluando la calidad de los estudios clínicos y, en mi opinión, esta es particularmente deficiente en los de psiquiatría. Las empresas financian dichos estudios, que se publican de forma selectiva y que suelen ser a corto plazo. Están diseñados para favorecer los resultados del medicamento y muestran tan pocos beneficios que es poco probable que los efectos secundarios compensen a largo plazo. (pág. 292)
Trastorno disfórico premenstrual
Sucedió, por ejemplo, con el «trastorno disfórico premenstural» (disforia). Durante las pruebas se determinó que las mujeres sin menstruación y los hombres padecían los mismos síntomas. A pesar de estos resultados, a las mujeres se las trataba con "Proz.." (fluoxetina), un inhibidor selectivo de la recaptación de serotonina (ISRS). Además, el mal humor solía atribuírseles a la menstruación.

EE: Distinguimos entre síndrome premenstural (SPM), que tiene una gran incidencia, y trastorno disfórico premenstrual (TDPM), que solo padecen entre un 3 y un 8 % de las personas. La línea que separa el SPM del TDPM es muy fina. Y esta última resulta «interesante» para los médicos...
Los investigadores afirman que una combinación determinada de ácidos grasos puede aliviar los síntomas y proponen un cambio en la dieta. Las personas afectadas deben evitar de forma estricta durante los últimos días antes de que comience su período los platos ricos en sal, el alcohol, el chocolate y la cafeína.
Déficit de atención/trastorno por déficit de atención con hiperactividad (TDAH), depresión y trastornos bipolares de tipo II
Otro ejemplo es el déficit de atención/trastorno por déficit de atención con hiperactividad (TDAH) en niños. Según el autor, en Estados Unidos son muchos los niños que tienen prescritos medicamentos para el trastorno por déficit de atención con hiperactividad (TDAH). En el año 2006, una cuarta parte de los niños tomaba este tipo de medicación en los campamentos de verano. Este número aumenta, mientras que la financiación de las escuelas se reduce.
Las depresiones aparecen en reacciones de duelo normales ante la pérdida de un ser querido, en crisis vitales tras la pérdida del trabajo o ante una separación, entre otras causas. No es de extrañar que, supuestamente, una cuarta parte de los estadounidenses adultos padezcan un trastorno mental.
La nueva «epidemia» son los trastornos bipolares de tipo II. Para este diagnóstico ya no hacen falta trastornos maníacos o psicóticos. Basta con haber padecido un episodio de depresión y una hipomanía de al menos cuatro días de duración. La hipomanía se caracteriza por un estado anímico animado que también se puede deber a los medicamentos.
En la página 300, el autor cita a Des Spencer, un médico de atención primaria británico que publicó «Adult attention deficit/hyperactivity disorder» (Déficit de atención en adultos/trastorno por déficit de atención con hiperactividad), BMJ 2011, 343d7244. En él, el doctor en medicina Des Spencer describió hasta qué punto la psiquiatría supone una mina de oro para la industria farmacéutica:
Buscan a un pequeño grupo de especialistas en instituciones de prestigio. La industria farmacéutica, que es un hacedor de reyes profesional, apoya las investigaciones de dichos especialistas. Esas investigaciones siempre dan como resultado que ciertos trastornos no se diagnostican o no se tratan lo suficiente, nunca lo contrario. Controlan los datos y limitan la duración del estudio. Emplean los medios de comunicación, sacan noticias y financian a grupos de pacientes. Pagan a los expertos honorarios muy altos, persuaden a políticos y consiguen que los expertos a los que apoyan asesoren al gobierno.
Un psiquiatra corrupto en una universidad estadounidense lo tuvo especialmente fácil. Escribió evaluaciones psiquiátricas sobre sus críticos y provocó su despido. Con esta y otras tácticas consiguió lanzar al mercado un dispositivo para estimular el nervio vago en pacientes depresivos.
El autor declara que, en el caso de los trastornos psiquiátricos y, especialmente, de la depresión, los chequeos preventivos no tienen sentido, ya que solo provocan que haya pacientes sanos a los que se prescribe medicación.
Antidepresivos, "Proz.." y paroxetina

La doctora en medicina LÖ: coincido con el autor en que tratar a personas sanas con antidepresivos es irresponsable y entiendo que hacerlo puede provocar un aumento de la agresividad y de las autolesiones. Nosotros solo tratamos depresiones severas: personas que, en muchos casos, ya han decidido qué tipo de suicidio prefieren, que no pueden trabajar, no tienen ningún tipo de contacto social, llevan semanas sin salir de la cama o no pueden dormir. Esto puede resultar muy duro para su entorno.
A estas personas se les puede ayudar con antidepresivos. He visto muchos suicidios sin tratamiento (solo puedo escribir de manera cínica que a los muertos les va bien), pero es raro que esto suceda si el paciente tiene prescritos ISRS. El autor declara que hay un fenómeno de interrupción del tratamiento, pero yo no lo he observado. Lo que sí he experimentado son pacientes que, pasados unos meses o unos años, vuelven a sufrir una depresión y que vuelven a necesitar tratamiento.
El autor también describe los pasos de la empresa Eli Lilly para conseguir la autorización para lanzar al mercado "Proz.." (fluoxetina). A saber: encubrimiento de los efectos secundarios, suicidios, agresividad en los pacientes sanos, soborno de funcionarios y expertos.
A pesar de las elevadas tasas de suicidio entre los niños, también se aprobó su prescripción. Asimismo, informa sobre los suicidios en personas que tenían prescrito "Cymbal..", duloxetina, un inhibidor selectivo de la recaptación de serotonina y noradrenalina (IRSN) en mujeres sanas que participaron en un estudio cuyo fin era, supuestamente, aprobar una droga para mejorar la incontinencia relacionada con el estrés.

La doctora en medicina LÖ: el autor recomienda a las personas depresivas practicar deporte en lugar de tomar medicación. En trastornos simples, estoy completamente de acuerdo. Sin embargo, ¿ha intentado convencer a una persona con depresión grave y sin medicación de que se dé un simple paseo? Yo sí, pero más bien en vano.
A continuación, el profesor y doctor en Medicina Peter C. Gøtzsche expone la paroxetina ("Pax..", "Serox..") y a la empresa GlaxoSmithKline, que no informó de que su medicamento provocase síndrome de abstinencia grave en el 30 % de los pacientes ni de que se produjeran intentos de suicido.
2.17. Empujar a los niños al suicido con pastillas para la felicidad
En 2001, GlaxoSmithKline publicó un estudio en niños y adolescentes (Study 329, en inglés, muy amplio). En el informe se afirmaba que el "pax.." ("Serox..") era muy efectivo y tenía efectos secundarios mínimos. El estudio era falso. La efectividad se había conseguido «maquillando» los datos en un subgrupo. Se ocultaron los efectos secundarios. Parte de los participantes eran personas ficticias o, tras el suicidio de algún sujeto, se asignó ese mismo número a otra persona.
El departamento de «expertos» recibió una gran suma de dinero de la empresa. Tras varios suicidios se prohibió su uso en niños y adolescentes.
"Citalopr.." de H. Lundbeck A/S en Dinamarca
Aquí nos encontramos frente a otra historia de «Evergreen» (perenne). "Citalopr.." de H. Lundbeck A/S en Dinamarca. Se trata de un esteroisómetro aislado (isometría). Cuando la patente de la mezcla racémica de "citalopr.." caducó, la empresa patentó la mitad activa de este superventas con el nombre de "Escitalopr.." ("Cipral..").
El «nuevo» medicamento costaba 19 veces más que el genérico del "citalopr..". En este caso, los expertos a sueldo también consiguieron demostrar que el fármaco era mejor que la versión de sí mismo
.
Antipsicóticos
Continúa con los antipsicóticos (neurolépticos).

La doctora en medicina LÖ: admito de buena gana la afirmación del autor de que los nuevos antipsicóticos no son mucho mejores o tienen menos efectos secundarios que los viejos. En los estudios comparativos, la dosis de los medicamentos antiguos se aumentaba enseguida o se administraban mal para que los nuevos medicamentos obtuvieran mejores resultados. Nadie prescribiría (esperemos) este tipo de medicamentos para trastornos que no sean lo suficientemente serios. Sin embargo, coincido con él en que a los pacientes les iría mejor si se retirasen todos los psicofármacos del mercado.
Me acuerdo perfectamente de una paciente que vino cuando acabábamos de abrir la consulta para que le prescribiésemos un medicamento antipsicótico. Al principio no nos quería decir por qué lo quería. Después nos confesó que había estado en dos hospitales psiquiátricos durante bastante tiempo. Desde que nuestro predecesor le había prescrito el fármaco, estaba muy bien.
Por desgracia, dicho medicamento había sido retirado del mercado por algún motivo y la mujer no quería tomar otros sustitutos. Unas semanas después, empezó a quemar las cosas del colegio de su hija y a lanzar los muebles por la ventana. Cuando un doctor se presentó en el lugar, pensó que era el demonio y lo quiso echar de casa. Después de una nueva y prolongada estancia en una institución psiquiátrica y nuevos medicamentos, vuelve a estar bien tras 20 años.
"Zypre.." (principio activo, olanzapina), un antipsicótico de la empresa Eli Lilly, es un viejo conocido, pero la empresa alegó que aumenta el nivel de colesterol en los perros menos que otros medicamentos que nunca llegaron al mercado.
El mayor estudio sobre la olanzapina se publicó 142 veces(!) y "Zypre.." se convirtió en el antipsicótico más vendido del mundo, a pesar de que no tenía ninguna ventaja en comparación con el "Haloperid..", a excepción de que el primero era siete veces más caro.
A pesar de los importantes efectos secundarios, como insuficiencia cardíaca, neumonía, aumento de peso severo y diabetes, "Zypre.." también se recomendó para niños y personas mayores.
Cuando la patente de "Proz.." caduó, Eli Lilly intentó comercializar "Zypre.." incluso contra la depresión.
2.18. Intimidación, amenazas y violencia para mejorar las ventas
Destapar las actividades delictivas de la industria farmacéutica es difícil y peligroso. Stanley Adams (enlace en inglés) antiguo empleado de la empresa farmacéutica de Basilea Hoffmann-La Roche, que informó a la Comisión Europea sobre el cártel vitamínico de Roche, terminó siendo acusado de espionaje y en una prisión suiza.
«Lo de Adams»
Willi Schlieder, comisario europeo de Competencia, reveló el nombre de Adams a Roche. Cuando la mujer de Adams se enteró de que a su marido podían esperarle 20 años en prisión, se suicidó. (pág. 353)

EE de Weltwoche:
«Cuando Gerber entró a reformar las cosas en 1978, ya sabía de las inclinaciones de Basler por fijar los precios. Y aún más: tuvo que afrontar el problema directamente. Una de sus primeras tareas como director de la empresa fue limpiar todo lo que quedó tras el escándalo de Adams. En 1970, Roche había obligado a sus grandes compradores de vitaminas a firmar «contratos de fidelidad» para asegurarse una cuota de mercado propia y alta. Stanley Adams, un empleado frustrado al que se le había negado un ascenso, entregó a la Comisión Europea una serie de documentos con los acuerdos ilegales. Roche tuvo que pagar una multa y el caso, que tuvo una gran repercusión mediática, terminó frente al Tribunal de Justicia Europeo apenas un año después de que Gerber hubiese asumido el puesto de director».
«A Gerber se le debió de advertir de que se habían incorporado los controles pertinentes y de que los reguladores de la competencia estaban imponiendo multas draconianas por todo el mundo. Pero no hizo nada. Así que, al parecer, se le escapó que entre los años 1989 y 1999 los principales gerentes de la división de vitaminas se reunían mensual o trimestralmente con representantes de «empresas de la competencia» como BASF o Rhône-Poulenc para comentar la facturación, volumen de ventas y mercados internacionales para las vitaminas».
«Bajo la atenta mirada de Henri B. Meier, un respetado experto financiero del país, se hizo caso omiso a cualquier teorema económico, ya que no había necesidad de bajar el precio en un mercado altamente competitivo en el que incluso se podía aumentar hasta en un 15 %»
El enlace «Adams-Affäre» (Escándalo de Adams) redirige a un artículo en línea del periódico alemán Zeit, «Allein gegen den Multi» de Wilfried Kratz, publicado el 27.01.84.
Eche un vistazo a la segunda página también.
En Estados Unidos, los denunciantes reciben grandes recompensas económicas. Seguramente las necesiten, pues nadie vuelve a darles trabajo.
Si un empleado se atreve a informar primero a la empresa, se arriesga a que le intimiden, difamen o amenacen para evitar que la noticia salga a la luz.
Grünenthal y la talidomida (Contergan))
Talidomida (Contergan): el médico que destapó por primera vez los numerosos y extraños defectos de nacimiento que provocaba la talidomida se vio perseguido durante diez años por la empresa Grünenthal, que le amenazó con demandarle. El juicio contra la empresa Astra, que fabricó la talidomida en Suecia, demostró ser difícil, pues resultó complicado encontrar expertos que quisieran declarar contra Astra.
En Estados Unidos, la empresa comercializó el medicamento sin que este estuviese aprobado. Después, contrató a todos los expertos en defectos de nacimiento que encontró para que no pudieran testificar a favor de las víctimas.
En Alemania nunca se llegó a condenar a nadie. La firma llegó a un acuerdo: unos 11 000 dólares por cada bebé nacido con malformaciones. En Reino Unido todo fue confidencial. Hubo que esperar 16 años para que por fin se pudiera escribir al respecto en la Unión Europea.
«Puede que tengamos que rastrearlos y machacarlos allí donde vivan»
Merck puso foco y presión de forma deliberada sobre aquellos médicos que hicieron preguntas incómodas acerca de "Vio..".
Unos días después de que Eric Topol testificase afirmando que el antiguo presidente de Merck, Raymond Gilmartin, había llamado al consejo de la clínica para la que trabajaba para quejarse sobre las opiniones vertidas por este sobre "Vio..", ("Top..") perdió su puesto como rector y director académico del departamento de Medicina de la Cleveland State University (Universidad de Cleveland).
Un correo interno de Meck sobre este tema: Puede que tengamos que rastrearlos y machacarlos allí donde vivan (pág. 357).

La doctora en medicina LÖ: «Estamos hablando de médicos, no de ratas».
Algunos mensajes de felicitación decían: «NEUTRALIZADO» o «DESACREDITADO».
El autor incluye otras citas de una reunión secreta y las compara con el libro 1984, una novela distópica de George Orwell (que en realidad se llamaba Eric Arthur Blair. Véase también Rebelión en la granja).
Un antiguo director de la FDA también intentó desacreditar a un subordinado, ya que este quería hacer público un estudio sobre los efectos secundarios de "Vio..".
Las empresas suelen actuar con mayor ferocidad cuando alguien descubre que han estado ocultando peligrosísimos efectos secundarios: llamadas amenazadoras, regalos fúnebres y macabros, coches vigilando la casa por las noches, fotos anónimas de los hijos de camino al colegio, etcétera. También han emprendido acciones legales, aunque los investigadores tuviesen todo el derecho a publicar su trabajo.
El ministro canadiense de salud terminó capitulando frente a las amenazas de AstraZeneca y retiró las directivas que afirmaban que los inhibidores de bombas de protones eran todos iguales. La revista médica alemana Zeitschrift für Allgemeinmedizin (Revista de medicina general, enlace en alemán) no se atrevió a publicar un artículo que contenía las mismas afirmaciones.
A un científico que protestó por la prescripción de hormonas durante la menopausia y a otro investigador que demostró que las nuevas píldoras anticonceptivas provocaban más trombosis que las antiguas se les amenazó con demandarlos.
Otro investigador recibió amenazas de muerte por querer hacer públicos los efectos secundarios sobre el sistema cardiovascular de un caro medicamento de GlaxoSmithKline en una conferencia. Y la lista no terminaría aquí. Incluso aunque una pequeña organización o individuo gane la demanda, los costes judiciales les perjudican más a ellos de lo que la multa perjudica a la empresa.
2.19. Los cuentos chinos de la industria, al descubierto
La industria farmacéutica repite hasta la saciedad cuentos chinos sobre sus actividades y motivaciones y consigue que el público, muchos médicos y políticos se los crean. Esto impide la creación de un sistema sanitario decente y sin corrupción.
Cuentos chinos: «Los medicamentos son caros porque los costes de descubrimiento y desarrollo también lo son»
En realidad, el precio de los medicamentos lo establece lo que la sociedad esté dispuesta a pagar por él y si la empresa consigue mantener a la competencia a raya (fijación de precios, etcétera). Dos universidades que reciben dinero de la industria afirman que sacar un nuevo medicamento al mercado cuesta 800 millones de dólares. Probablemente, el coste real sea de unos 100 millones. Muchos medicamentos los desarrollan organismos públicos y lo más caro suele ser la campaña publicitaria.
El autor señala este y otros costes como, por ejemplo: Schering compró una hormona para tratar los síntomas de la menopausia y después la vendió incrementando el precio en un 7000 %. (pág. 373)
Si los nuevos medicamentos fuesen tan buenos como la industria nos quiere hacer creer, no sería necesario sobornar a los médicos para que los prescribiesen.
Cuentos chinos: «Si no usamos los medicamentos costosos, la innovación morirá»
Desde los años 80, los beneficios de la industria farmacéutica han alcanzado niveles estratosféricos, pero los medicamentos que llegan al mercado cada vez son menos innovadores. (pág. 375)
En Nueva Zelanda, el gobierno decidió en 1993 que, en medicamentos del mismo tipo como, por ejemplo, los AINE o los ISRS que tuviesen efectos similares, pagaría el mismo precio, algo que controlaría la autoridad competente en el país. Esta política tuvo un gran impacto, pues a partir de entonces las estatinas se pusieron a disposición de los pacientes por la mitad de lo que costaban en Australia y los genéricos, por una cuarta parte del precio en Canadá. Y aquel año, ese país de solo 4,4 millones de habitantes consiguió ahorrar mil millones de euros.
Cuentos chinos: «En los medicamentos caros, el ahorro es mayor que el coste»
Los economistas de la industria farmacéutica argumentan que el ahorro que se produce con la reducción de las ausencias al trabajo por enfermedad y el retraso de la jubilación es mayor que los costes del medicamento. En economía es fácil probar una cosa y todo lo contrario.
En Dinamarca, el director de la autoridad sanitaria nacional afirmó que es extraño que, sin importar cuál sea el nuevo medicamento, la empresa siempre es capaz de presentar cálculos de rentabilidad y eficiencia que prueben el ahorro según ausencias en el trabajo, jubilación temprana y lo que se tercie en relación con el coste del medicamento.
Cuentos chinos: «La industria financia estudios que desencadenan descubrimientos científicos»
La investigación básica que hace avanzar a la medicina moderna tiene lugar, casi de manera exclusiva, en el sector no comercial: universidades, institutos de investigación y laboratorios nacionales.
Los tres grandes descubrimientos del siglo XX (penicilina, insulina, vacuna contra la poliomielitis) se realizaron en laboratorios financiados con fondos públicos. Para los cinco medicamentos más vendidos en 1995, 16 de las 17 publicaciones que condujeron a su descubrimiento se realizaron fuera de la industria.
Más de cuatro quintas partes de la investigación básica que se realiza para descubrir nuevas vacunas y medicamentos se lleva a cabo gracias a fondos públicos. (pág. 378)
Cuentos chinos: «Las empresas farmacéuticas compiten entre ellas en un mercado libre»
No hay libre mercado cuando se trata de productos subvencionados en gran medida por el contribuyente, más cuando existe tanto fraude y los delitos están tan extendidos.
En este caso, el doctor Gøtzsche aporta algunas de las experiencias con la industria farmacéutica que ha vivido en su consulta.
Cuentos chinos: «Las asociaciones entre la industria y las administraciones son beneficiosas para los pacientes»
Aunque ambos lados pueden beneficiarse de este tipo de asociaciones, en general suelen ser perjudiciales para el paciente. La noción de que la industria farmacéutica y los sistemas de salud comparten objetivos comunes no es más que un mero truco publicitario.
A este respecto, el autor se explaya en casi dos páginas y expone con total claridad ciertas prácticas y alegatos vacíos extraídos, sobre todo, del libro «Bad Pharma: How drug companies mislead doctors and harm patients» de Ben Goldacre, Londres: Fourth Estate 2012. En español, «Mala farma: Cómo las empresas farmacéuticas engañan a los médicos y perjudican a los pacientes», publicado por Paidós Ibérica en 2013.
Cuentos chinos: «Los estudios clínicos se llevan a cabo para mejorar el tratamiento de los pacientes»
Los estudios se crean para maximizar la facturación o para encontrar el mejor método para retrasar la aparición de una enfermedad o tratarla.
Los estudios de la industria farmacéutica tienen fines publicitarios. Cuando los resultados no son los esperados, la empresa los mantiene en secreto o los manipula antes de publicarlos.
Sin acceso a los datos limpios es muy difícil descubrir estas prácticas. Además, las multas son pequeñas y su reputación apenas se ve dañada.
Cuentos chinos: «Necesitamos diferentes medicamentos del mismo tipo porque la respuesta de los pacientes varía»
El doctor Gøtzsche explica: He oído este mismo argumento muchas veces de la boca de diferentes médicos que repiten una y otra vez lo que los representantes farmacéuticos les dicen, sin pararse a pensar si esas afirmaciones son verdaderas o no. Puede ser cierto en algunos casos, raros, pero no hay ningún dato convincente que lo respalde.
(pág. 382 - EE: si el cuerpo responde de forma positiva, es que el medicamento está actuando).
Märchen: Cuentos chinos: «No utilizo genéricos porque no tienen la misma eficacia»
Las autoridades sanitarias exigen a los fabricantes de genéricos estudios comparativos que demuestren que los genéricos y los medicamentos originales son equivalentes. Para ello, se mide el nivel de la sustancia activa en la sangre.
Muchos médicos se creen esta tontería (que la eficacia es diferente), que además ha sido rechazada una y otra vez por científicos sin conflictos de intereses que han probado la biodisponibilidad.
Cuentos chinos: «La industria paga la formación de los médicos porque los fondos públicos no lo hacen»
Sería una oferta muy generosa, pero la formación objetiva no va de la mano con los intereses de las empresas. De lo contrario, tendrían que decir en más de una ocasión: ¡Tome el producto de la competencia, que es mejor y más barato! En realidad, el interés de las empresas cuando «forman» a los médicos no es otro que el de mejorar su cuota de mercado.
2.20. El fracaso del sistema pide una revolución
Si la salud de los pacientes fuese el objetivo principal, algunos de los miles de millones que se están invirtiendo en costosos medicamentos para reducir los niveles de colesterol podrían emplearse de formas mucho más eficientes: Por ejemplo, podrían utilizarse para sufragar los costes de campañas contra el tabaquismo o que animasen a practicar más deporte.
En este caso, el autor cita «Selling Sickness» (Vendiendo enfermedades), de Moynihan y Cassels.
 | EE: En Youtube hay una serie de vídeos sobre las prácticas en la comercialización y en la producción. Aquí, el vídeo expone algunos datos repugnantes sobre los productos de McDonald’s. Por desgracia, solo está disponible en inglés. Duración 7:08 minutos. |
Los medicamentos son, por detrás de las enfermedades cardíacas y del cáncer, la tercera causa de muerte

EE: «Selling Sickness (enlace en inglés): How the World's Biggest Pharmaceutical Companies are Turning us All into Patients» de Ray Moynihan (enlace en inglés) y Alan Cassels. (Vendiendo enfermedades: cómo las grandes empresas farmacéuticas nos están convirtiendo a todos en pacientes). Nation Books. (24 de junio de 2005). No hemos encontrado traducción al español.
Alan Cassels también ha escrito, entre otros: «Seeking Sickness: Medical Screening and the Misguided Hunt for Disease», editorial Greystone Books, 1ª edición. (24 de julio de 2012). (Vendiendo enfermedades: exámenes médicos que van a la caza de la enfermedad por los motivos equivocados).
El autor destaca que los medicamentos son, solo por detrás de las enfermedades cardíacas y del cáncer, la tercera causa de muerte. En este caso sí que hay datos razonables disponibles y en algunos de ellos se expone que en Estados Unidos mueren al año 100 000 personas debido a los medicamentos que tomaban, aunque lo hiciesen de forma correcta. Otros 100 000 lo hacen por fallos como, por ejemplo, dosis demasiado altas o su consumo a pesar de las contraindicaciones.
Un estudio noruego cuidadosamente realizado concluyó que, del total de fallecidos en los hospitales, el 9 % se debe directamente a los medicamentos que se les ha administrado. Y otro 9 %, de forma indirecta. La Comisión Europea estima que unos 200 000 ciudadanos europeos mueren debido a los efectos secundarios (lo que tiene un costo de casi 79 mil millones de euros).

La doctora en medicina LÖ: si estas personas no hubiesen padecido la enfermedad para la que se les prescribió dicho medicamento o no se lo hubiesen tomado, ¿habrían muerto también? Por supuesto, coincido con el autor en que necesitamos menos y mejores medicamentos y que hay situaciones que no pueden ni deben tratarse. Estados Unidos gasta casi el doble que los países europeos en sanidad y 2,7 veces más en medicamentos. Sin embargo, su esperanza de vida es más baja. Un estudio concluyó que la mortalidad desciende en un 60 % cuando el número de médicos de atención primaria asciende en un 20 %. En Suiza, por ejemplo, este número está a la baja.
¿Cuántos medicamentos necesitamos realmente y a qué precio?
El uso de medicamentos de baja calidad para tratar la hipertensión arterial ha provocado insuficiencia cardíaca en aproximadamente 40 000 pacientes estadounidenses.
(pág. 165)
Los datos respaldan que los medicamentos son una de las causas de muerte más habitual
Algunos medicamentos son innecesarios y para otros hay alternativas más económicas. Los datos respaldan que los medicamentos son una de las causas de muerte más habitual:
En este momento, los medicamentos que suelen prescribirse para tratar las arritmias cardíacas han costado la vida a 50 000 personas en Estados Unidos.
(pág. 202)Para el año 2004, el "rofecox.." había provocado la muerte de unos 120 000 pacientes en todo el mundo debido a las trombosis mortales provocaba.
(pág. 250Para el año 2004, el "calecox.." había causado la muerte de aproximadamente 75 000 pacientes en todo el mundo debido a las trombosis mortales.
(pág. 258)En Estados Unidos, los AINE son los responsables cada año de unas 20 000 muertes por úlceras gástricas o intestinales.
(pág. 260)Para el año 2007, la olanzapina se había cobrado la vida de unas 200 000 personas en todo el mundo.
(pág. 351)Además, cada año millones de personas sufren graves reacciones adversas a los medicamentos, lo que les impide trabajar.
Un modelo con ánimo de lucro es un modelo equivocado
Cuando el director de una empresa farmacéutica «gana» 531 veces más que un empleado de la misma empresa, nos resulta complicado llegar a imaginarnos tales cantidades.
Una industria orientada puramente por el ánimo de lucro en la que el precio de las acciones es mucho más importante que producir medicamentos buenos y económicos no será quien salve nuestro sistema de salud.
Las exageraciones de la industria
Un ejemplo de un medicamento que llegó al mercado por los beneficios y no porque fuera realmente necesario es la eflornitina (aminoácido dibásico, precursor de IGF).
La desarrolló la empresa Aventis (que más tarde pasaría a llamarse Sanofi-Aventis y después, solo Sanofi). Era ineficaz contra el cáncer pero excelente contra la enfermedad del sueño (tripanosomiasis africana). Puesto que los pacientes que padecen esta enfermedad suelen ser pobres, Aventis dejó de producirlo.

Volvió a salir al mercado como medicamento para el hirsutismo (pero no es una crema depilatoria). (pág. 394, EE: véase Pharma-Kritik 30, número 12, PK239).
El doctor Gøtzsche nos enseña lo exagerada que resulta esta industria:
En 2010, cuatro de los diez directivos mejor pagados de Estados Unidos pertenecían a la industria sanitaria o farmacéutica. John Hammergren, el mejor pagado, era el director general de McKesson Corp y ganaba en total 145 millones de dólares. Si al pobre le hubiesen despedido, habría recibido una indemnización de 469 millones.
Las patentes no son buenas si impiden que los medicamentos se comercialicen a precios razonables que la población se pueda permitir.

EE: Sobre todo cuando somos los contribuyentes los que sufragamos el proceso de desarrollo. El autor sugiere algunas alternativas innovadoras.

Comentarios