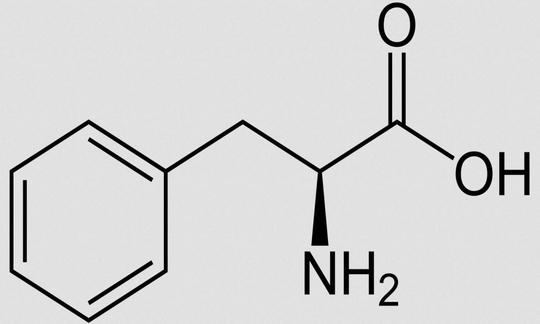
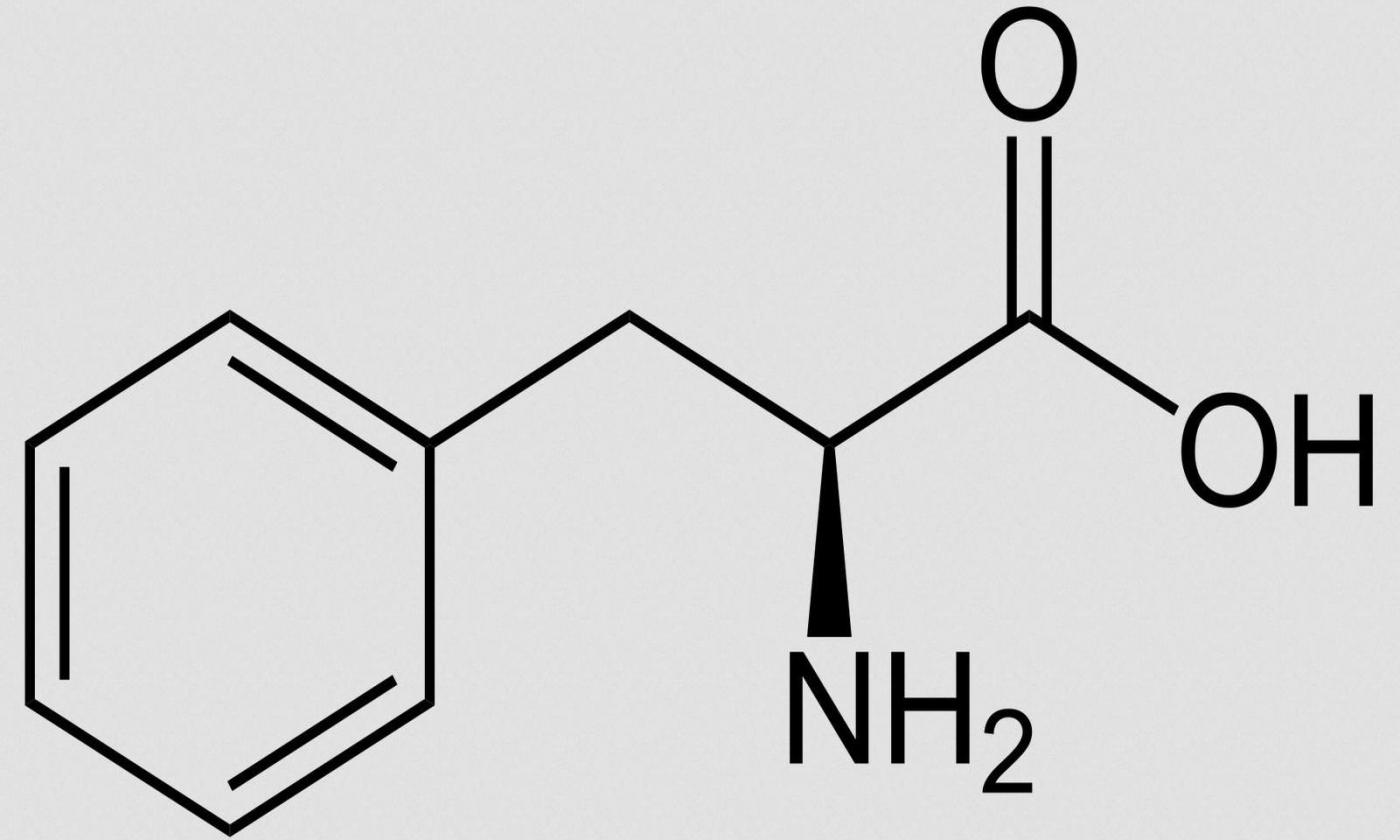
Fenilalanina (Phe, F)
Conclusioni:
una dieta naturale che include legumi, noci e semi copre perfettamente le esigenze della leucina. I bambini possono soffrire di carenze se smettono di allattare troppo presto.
L'essere umano usa 21 aminoacidi proteinogenici. Questi fanno parte delle proteine . Il corpo può adattare fino a due proteine ai suoi bisogni, sebbene tradizionalmente ci siano otto aminoacidi essenziali.
Fonti: i
legumi contengono principalmente molta fenilalanina, come i semi di soia (1998 mg / 100 g) o i fagioli (1260 mg). Anche semi come sesamo (1010 mg) e semi di lino (960 mg) e noci come mandorle (1130 mg) o noci (711 mg) sono ricchi di questo aminoacido, come nel caso dei cereali integrali. D'altra parte, anche le verdure e le bacche sono circa quella quantità, ma la frutta è persino indietro. 1
Carne, pesce e uova (680 mg) o latte (solo 158 mg) contengono meno fenilalanina rispetto a semi di soia, semi di zucca, piselli secchi o mandorle.
Ingedriente | Proteine g / 100 g (USDA) | Fenilalanina mg / 100 g | % fenilalanina proteica |
Semi di soia secchi | 36,49 g | 2122 mg | 5,8% |
Tubi Di Zucca | 30,23 g | 1733 mg | 5,7% |
| 24,55 g | 1132 mg | 4,6% | |
| 22,57 g | 1130 mg | 5,1% | |
| 15,23 g | 711 mg | 4,7% | |
| 13,7 g | 646 mg | 4,7% | |
Riso non pelato | 7,94 g | 410 mg | 5,2% |
- Conservazione e perdite durante la cottura:
riscaldare i piatti denatura le proteine e ne trasforma le proprietà Questo si osserva nei processi di coagulazione-flocculazione. Un esempio di questo sono le uova fritte, che sono denaturate dal calore della padella. L' ossidazione delle proteine di un amminoacido attraverso specie reattive dell'ossigeno può influenzare significativamente le sue funzioni.
Nutrizione / salute: gli
aminoacidi sono, tra le altre cose, parti di proteine . La fenilalanina (Phe, F) è una delle otto (con istidina e arginina , dieci nel caso dei bambini) amminoacidi essenziali del corpo umano, noti fino ad ora come aminoacidi o proteine essenziali.
Nel frattempo, è noto che il corpo può eseguire irreversibilmente la transaminazione di lisina e treonina e che questi sono gli unici due essenziali.3-114 Le persone che mangiano vegan ricevono in media il doppio di treonina e hanno buoni livelli di lisina. Abitudini alimentari speciali, p. Ad esempio, una dieta a base di frutta o simili può, nel tempo, presentare delle carenze, sebbene non compaiano sintomi riconoscibili.
Essenziale significa che il nostro corpo non può produrlo (sintetizzarlo) da solo, ma è necessario in determinate quantità. In effetti, la fenilalanina può anche essere sostituita in una certa misura dall'amminoacido tirosina non essenziale.
Quantità giornaliera necessaria a lungo termine:
Traduzione dell'articolo di Wikipedia in tedesco: poiché il corpo utilizza la fenilalanina per produrre l'amminoacido tirosina, la quantità necessaria di fenilalanina dipende dalla quantità di tirosina che consumiamo nella nostra dieta abituale. In una dieta normale, entrambi gli aminoacidi sono presenti in determinate proporzioni. Almeno nel caso di adulti sani, è anche possibile soddisfare i bisogni di tirosina solo con la sintesi di fenilalanina. La normale dose giornaliera dovrebbe essere di circa 14 milligrammi per chilo di peso corporeo (in un adulto).
Secondo il libro Scientific Tables. Documenta Geigy , vol.2, p. 232, la quantità giornaliera totale raccomandata di fenilalanina e tirosina è di 16 mg / kg di peso corporeo, incluso un supplemento del 30% per possibili variazioni individuali. Per una persona che pesa 75 kg, sarebbe 1,2 g / giorno. Ci sono studi recenti che raccomandano persino di prenderne di meno.
Se abbiamo un eccesso di tirosina, avremo bisogno di circa 9 mg di fenilalanina per chilo di peso corporeo al giorno. In un rapporto di fenilalanina e tirosina di 60:40, l'uso di entrambi gli aminoacidi sarebbe ottimale.
Sintomi di carenza e cause:
in una dieta equilibrata, di solito non si verificano carenze di fenilalanina. Una dieta vegana naturale soddisfa in modo soddisfacente le esigenze della fenilalanina e, più sport fai, più mangi. I bambini possono soffrire di questo tipo di carenza se smettono di allattare troppo presto e non vengono nutriti correttamente.
Una carenza prolungata nel tempo può ridurre l'efficienza, l'appetito e causare disturbi metabolici. Alcune malattie derivate dalla mancanza di proteine o dal consumo di energia in generale sono kwashiorkor e marasmus , che si verificano sempre più nel mondo occidentale.
- Consumo eccessivo :
elevate concentrazioni di fenilalanina si verificano quando la degradazione o la conversione di essa in altre sostanze non funziona correttamente. Questo è qualcosa che accade, ad esempio, alle persone che soffrono di fenilchetonuria , un disturbo genetico. In questa situazione, l'organismo non degrada affatto la fenilalanina e si concentra nel sangue in quantità elevate, il che ha un effetto negativo sulla funzione cerebrale.
Le persone con fenilchetonuria dovrebbero prestare attenzione alla fenilalanina che la loro dieta contiene per la vita. Ad esempio, nell'etichetta alimentare del dolcificante aspartame è indicato che "contiene fenilalanina", poiché rilascia l'amminoacido durante la digestione.
In caso di problemi con la funzionalità renale, è necessario seguire una dieta a basso contenuto proteico per evitare la produzione e l'accumulo di urea nei reni a causa della degradazione degli aminoacidi. Il libro Lo studio della Cina riflette con prove che normalmente il nostro corpo ha un eccesso di proteine e non mancano (vedi questa recensione dettagliata del libro ): sono passati solo un paio d'anni da quando gli scienziati hanno scoperto che le proteine animali, finora considerata la migliore qualità (da un punto di vista biologico), non è una fonte di salute, ma piuttosto il contrario.
Funzioni nel corpo:
- La fenilalanina e la tirosina, che dipendono dalla prima, contribuiscono alla sintesi di importanti proteine endogene, come il neurotrasmettitore dopamina, l'adrenalina, il pigmento cutaneo della melanina o l'ormone tiroxina . La fenilalanina migliora le prestazioni della memoria e riduce l'appetito. 2, 3
- A differenza di altri aminoacidi, la fenilalanina svolge non solo funzioni nel corpo nella sua forma naturale L, ma anche nella sua forma D. I farmaci usano la fenilalanina sintetica L o D (DLPA), cioè una miscela racemica , come analgesico o per trattare le depressioni 2, 3
Assorbimento e metabolismo: la
digestione delle proteine ingerite inizia nello stomaco grazie alla pepsina . Divide le proteine in peptidi . Le seguenti divisioni individuali di aminoacidi si verificano nell'intestino tenue con l'azione delle peptidasi . Il fegato converte la fenilalanina in tirosina, un aminoacido non essenziale. Se la quantità di fenilalanina non è sufficiente, il corpo utilizza invece la tirosina.
Conservazione, consumo e perdite:
tra il 70 e l'80% degli aminoacidi liberi si trovano nel muscolo scheletrico e, in percentuale inferiore, nel plasma sanguigno . L'organo centrale per la regolazione degli aminoacidi è il fegato. C'è degradazione o deaminazione e conversione in urea per prevenire effetti citotossici.
Struttura: la
fenilalanina è un alfa aminoacido chirale aromatico con una catena laterale idrofobica. La fenilalanina è strutturalmente derivata dall'alanina ed è anfipatica.
Wikipedia: L-fenilalanina può essere trasformata, mediante una reazione catalizzata dall'enzima fenilalanina idrossilasi, in tirosina.
Altri nomi di fenilalanina: D-fenilalanina; DL-fenilalanina; L-fenilalanina. Formula molecolare: C 9 H 11 NO 2 . Forma abbreviata: Phe, F.
Bibliografia / fonti:
- Dipartimento dell'Agricoltura degli Stati Uniti. Informazioni nutrizionali sugli alimenti.
- Kasper Heinrich und Burghardt Walter: Ernährungsmedizin und Diätetik; 11a edizione (2009); Elsevier GmbH, editore Urban & Fischer, Monaco di Baviera.
- Biesalksi Hans Konrad e Peter Grimm: Tashenatlas der Ernährung; 6a edizione (2015); Casa editrice Georg Thieme, Stoccarda e New York.
- OMS: fabbisogno proteico e di aminoacidi nell'alimentazione umana. Serie di relazioni tecniche: 935; 2002.
Per questa ricetta è necessario immergere i fagioli la sera prima. Nel libro c'è un'insalata di tarassaco che si combina idealmente con questo piatto.
Questo peperoncino borlotti è un piatto smussato che può essere modificato a piacere e non lascerà nessuno insoddisfatto.
Queste crocchette di anacardi affumicate sono servite con barbabietola glassata nel porto e un'emulsione all'arancia e sono un'alternativa vegana a questa tradi
I cianobatteri spirulina (polvere, ecc.) non possono praticamente mai essere acquistati crudi. A causa del loro pigmento blu, in precedenza venivano classificat
I granuli di soia sono costituiti da semi di soia macinati, sgrassati e riscaldati: non sono mai crudi! Per il suo contenuto proteico e la sua consistenza è con
Il lievito di birra ha un sapore speziato, leggermente di formaggio. Vengono quindi utilizzati per condire o come sostituto del formaggio nelle pietanze. Argome





Commenti